
��12�֣��״�����Ҫ�Ļ�ѧ��ҵ����ԭ�Ϻ�Һ��ȼ�ϡ���ҵ�Ͽ�����CO��CO2������ȼ�ϼ״�����֪�״��Ʊ����йػ�ѧ��Ӧ�Լ��ڲ�ͬ�¶��µĻ�ѧ��Ӧƽ�ⳣ�����±���ʾ��
��ѧ��Ӧ | ƽ�ⳣ�� | �¶ȣ��棩 | |
500 | 800 | ||
��2H2(g)+CO(g) | K1 | 2.5 | 0.15 |
��H2(g)+CO2(g) | K2 | 1.0 | 2.50 |
��3H2(g)+ CO2(g) | K3 | ||
��1����Ӧ���� ������ȡ����ȡ�����Ӧ��
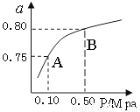
��2��ij�¶��·�Ӧ����H2��ƽ��ת���ʣ�a������ϵ��ѹǿ(P)�Ĺ�ϵ��ͼ��ʾ����ƽ��״̬��A�䵽Bʱ��ƽ�ⳣ��K(A) K(B)�����������������������
��3���ݷ�Ӧ����ڿ��Ƶ���K1��K2��K3֮��Ĺ�ϵ����K3= ����K1��K2��ʾ������500�桢2L���ܱ������У����з�Ӧ�ۣ����ijʱ��H2��CO2�� CH3OH��H2O�����ʵ����ֱ�Ϊ6mol��2 mol��10 mol��10 mol����ʱv(��) v(��) ���������=��������
��4��һ���¶��£���3 L�ݻ��ɱ���ܱ������з�����Ӧ�ڣ�
��֪c(CO)�뷴Ӧʱ��t�仯���ߢ���ͼ��ʾ������t0ʱ�̷ֱ�ı�һ�����������ߢ��Ϊ���ߢ�����ߢ�
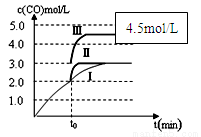
�����ߢ��Ϊ���ߢ�ʱ���ı�������� ��
�����ߢ��Ϊ���ߢ�ʱ���ı�������� ��

| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ�������и�����ѧ�ڵڶ�������������ۻ�ѧ�Ծ��������棩 ���ͣ�ѡ����
�������ӷ�Ӧ����ʽ�������
A����Na2SiO3��Һ����μ�������ϡ���SiO32��+ 2H+��H2SiO3�����壩
B��ϡFe(NO3)2��Һ�м���ϡ���Fe2����4H����NO3-= Fe3����NO����2H2O
C����CuƬ����ϡ�����У�3Cu + 8H��+2NO3����3Cu2+ +2NO��+ 4H2O
D����NH4Al(SO4)2��Һ�м��������Ba(OH)2ϡ��Һ��NH4+ + Al3+ + 2SO42�� + 2Ba2+ + 5OH����2BaSO4��+ NH3��H2O + AlO2��+ 2H2O
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ������ʡμ���и�����ѧ������⣨һģ����ѧ�Ծ��������棩 ���ͣ�ѡ����
�ں���4 mol HCI��1 mol MgSO4�Ļ����Һ����ժ����Ba(OH)2��Һ�������ij�������m�����Ba(OH)2���ʵ���n֮��Ĺ�ϵ��ͼ������˵������ȷ����
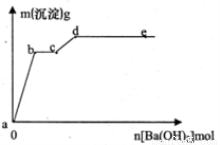
A��a��bʱ�ij����ijɷ�ֻ��BaSO4
B��b��cʱ���������ӷ�ӦΪ: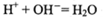
C��d��ʱ�����Ba(OH)2�����ʵ���Ϊ3mol
D��d�����Һ�����ӵ����ʵ���:Ba2��һ������OH��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ�������ʡ�绯�и�����һ��ģ�⿼�����ۻ�ѧ�Ծ��������棩 ���ͣ������
(14��)�����⻯��NH3��N2H4���ڹ�ũҵ���������պ���������й㷺Ӧ�á�
��1��Һ����Ϊһ��DZ�ڵ��������ȼ����Խ��Խ���о���Ա���ӡ����ڰ�ȫ�ԡ��۸�ȷ���ϻ�ʯȼ�Ϻ���ȼ�����Žϴ�����ơ�����ȼ��ʵ���漰����������صķ�Ӧ��
��4NH3(g)��5O2(g)��4NO(g)��6H2O(l)  H1
H1
��4NH3(g)��6NO(g)��5N2(g)��6H2O(l)  H2
H2
��Ӧ4NH3(g)��3O2(g)��2N2(g)��6H2O(l)  H�� ��(���ú���
H�� ��(���ú��� H1��
H1�� H2��ʽ�ӱ�ʾ)
H2��ʽ�ӱ�ʾ)
��2���ϳɰ�ʵ���У������Ϊ3 L�ĺ����ܱ������У�Ͷ��4 mol N2��9 mol H2��һ�������ºϳɰ���ƽ��ʱ���ı��¶Ȳ�õ��������±���ʾ��
�¶�(K) | ƽ��ʱNH3�����ʵ���(mol) |
T1 | 2.4 |
T2 | 2.0 |
��֪���ƻ�1 mol N2(g)��3 mol H2(g)�еĻ�ѧ�����ĵ�������С���ƻ�2 mol NH3(g)�еĻ�ѧ�����ĵ�������
����T1 T2(���������������=��)
����T2 K�£�����10min�ﵽ��ѧƽ��״̬����0~10min��H2��ƽ������v(H2)= ��ƽ��ʱN2��ת���ʦ�(N2)= ��
������ͼ��ֱ�����ʱ�(H)���������ƽ����Է�������( )��N2���������(N2)�������ܶ�(��)�뷴Ӧʱ��Ĺ�ϵ��������ȷ���ܱ����ÿ��淴Ӧ�ﵽƽ��״̬���� ��
)��N2���������(N2)�������ܶ�(��)�뷴Ӧʱ��Ĺ�ϵ��������ȷ���ܱ����ÿ��淴Ӧ�ﵽƽ��״̬���� ��
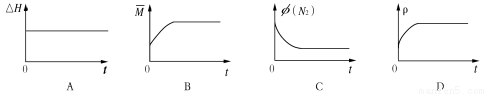
��3��ijN2H4(�»�����)ȼ�ϵ��(�����ȶ�������Ⱦ������)ԭ����ͼ1��ʾ��
��M�������ĵ缫��ӦʽΪ ��
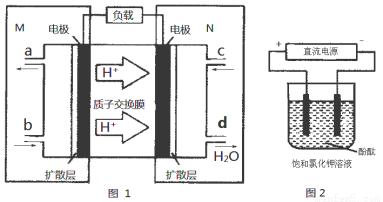
���������������Դ����ͼ2װ�õ�ⱥ���Ȼ�����Һ(�缫��Ϊ���Ե缫)���豥���Ȼ�����Һ���Ϊ500 mL������Һ��pHֵ��Ϊ13ʱ(�ڳ����²ⶨ)������ȼ�ϵ�ص�����������Ϊ80%����������N2H4������
Ϊ g(������Һ���ǰ���������)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ�������ʡ�绯�и�����һ��ģ�⿼�����ۻ�ѧ�Ծ��������棩 ���ͣ�ѡ����
��ѧ������������ɳ�����չ������ء������й�˵������ȷ����
A��������Ч���ܡ�̫���ܵ����͵綯�������Խ�����л�����β���ŷ�����
B���߿ճ���������̫�������ߣ�������������Ϳչ�����������Ⱦ���壬��������Σ��
C��PM2.5��ʾÿ����������ֱ��С�ڻ����2.5�Ŀ�����ĺ�����PM2.5ֵԽ�ߣ�������ȾԽ����
D���ޡ��顢��ë���ϳ���ά��ȫȼ�ն�ֻ����CO2��H2O���ʶԻ����������Ⱦ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ�꽭��ʡ��У�����ڶ����������ۻ�ѧ�Ծ��������棩 ���ͣ�ѡ����
��֪A��B��C��D��E�Ƕ�����ԭ���������������5��Ԫ�أ�Aԭ����Ԫ�����ڱ���ԭ�Ӱ뾶��С��B��Eͬ���壬��E��ԭ��������B��������C��D�ǽ��������ǵ����������������ˮ������˵���������
A���ȶ��ԣ�A2B��A2E
B����ҵ�ϳ��õ�ⷨ�Ƶ�C��D�ĵ���
C�������ӵİ뾶��C��D��E��B
D������D������ұ��ijЩ���۽���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015����ʡ��ԭ�и�һ��ѧ�ڵ�һ���¿���ѧ�Ծ��������棩 ���ͣ������
(12��)�ڻ�ѧ��Ӧ�У�ֻ�м�����������ƽ�������ߵö�ķ�Ӧ����ӷ�����ײʱ�ſ��ܷ�����ѧ��Ӧ����Щ���ӱ���Ϊ����ӡ�ʹ��ͨ���ӱ�ɻ���������ṩ������ȵ������л�ܣ��䵥λͨ����kJ��mol-1��ʾ��������۲���ͼ��Ȼ��ش����⡣
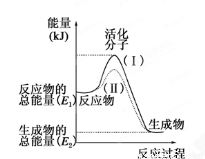
��1��ͼ����ʾ��Ӧ��________(����ȡ����ȡ�)��Ӧ��
��2����֪��1mol H��H����1mol I��I��1mol H��I���ֱ���Ҫ���յ�����Ϊ436kJ��151kJ��299kJ������1mol������1mol �ⷴӦ����HI��________(��ų��������ա�)________kJ���������ڻ�ѧ��Ӧ�����У��ǽ�___ ___ת��Ϊ___ _____��
��3��50mL 0.50molL��1������50mL 0.55molL��1 NaOH��Һ��ͼʾ��װ���н����кͷ�Ӧ��ͨ���ⶨ��Ӧ�����е������ɼ����к��ȣ��ش��������⣺
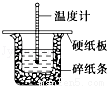
�ٴ�ʵ��װ���Ͽ���ͼ����ȱ�ٵ�һ�ֲ�����Ʒ�� ��
���ձ���������ֽ���������� ��
�۴��ձ����粻��Ӳֽ�壬��õ��к�����ֵ ���ƫ����ƫС������Ӱ�족����
��ʵ���и���60mL 0.50molL��1�����50 mL 0.55molL��1 NaOH��Һ���з�Ӧ��������ʵ����ȣ����ų������� �����ȡ�����ȡ����������к��� �����ȡ�����ȡ������������ɣ� ��
������ͬŨ�Ⱥ�����İ�ˮ����NaOH��Һ��������ʵ�飬��õ��к��ȵ���ֵ�� �����ƫ����ƫС������Ӱ�족��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015����ʡ��ԭ�и�һ��ѧ�ڵ�һ���¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
�������뾶֮�ȴ���1����
A��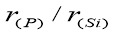 B��
B��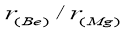
C�� D��
D��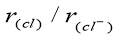
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ������ʡ����������У������ѧ�����������ۻ�ѧ�Ծ��������棩 ���ͣ�ѡ����
ʵ���ҴӺ��廯��ķ�Һ����ȡ�嵥�ʣ�����˵�����ܴﵽʵ��Ŀ�ĵ���
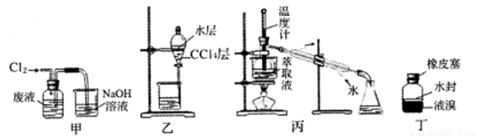
A����װ�ü�������Һ�е��廯��
B����װ���ҷ���CCl4���ˮ��
C����װ�ñ�����CCl4��Һ��
D������������������Һ��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com