
下列说法正确的是()
①用丁达尔效应可以区分食盐水和淀粉溶液
②一种盐和另外一种盐反应一定生成两种新盐
③与Al反应且只产生H2的溶液中能大量存在:NH4+、Na+、Fe2+、NO3﹣
④由CaCO3的溶解度小于Ca(HCO3)2,可推出Na2CO3的溶解度小于NaHCO3
⑤向溶液中滴入盐酸,无现象,再加氯化钡溶液,可检验溶液中是否含有SO42﹣
⑥标准状况下,0.5NA个NO分子与0.5NA个O2分子混合后的体积约为22.4L.
A. ①③ B. ①④ C. ①⑤ D. ①⑥
考点: 分散系、胶体与溶液的概念及关系;酸、碱、盐、氧化物的概念及其相互联系;阿伏加德罗常数;难溶电解质的溶解平衡及沉淀转化的本质;离子共存问题.
分析: ①胶体具有丁达尔现象,溶液不具有;
②硫酸氢钾与亚硫酸氢钾反应生成硫酸钾;
③使Al溶解产生H2的溶液,为非氧化性酸或强碱溶液;
④相同条件下,Na2CO3的溶解度大于NaHCO3;
⑤检验硫酸根离子,先加盐酸酸化,排除干扰;
⑥NO和O2混合气体反应生成二氧化氮,气体物质的量小于1mol,结合V=nVm分析.
解答: 解:①胶体具有丁达尔现象,溶液不具有,则用丁达尔效应可以区分食盐水和淀粉溶液,故正确;
②硫酸氢钾与亚硫酸氢钾反应生成硫酸钾,则一种盐和另外一种盐反应不一定生成两种新盐,故错误;
③使Al溶解产生H2的溶液,为非氧化性酸或强碱溶液,酸溶液中Al、Fe2+、NO3﹣发生氧化还原反应不生成氢气,碱溶液中不存在NH4+、Fe2+,故错误;
④相同条件下,Na2CO3的溶解度大于NaHCO3,CaCO3的溶解度小于Ca(HCO3)2,故错误;
⑤检验硫酸根离子,先加盐酸酸化,排除干扰,试剂的顺序及选择酸化的酸均合理,故正确;
⑥NO和O2混合气体反应生成二氧化氮,气体物质的量小于1mol,标况下由V=nVm可知,体积小于22.4L,故错误;
故选C.
点评: 本题考查较综合,涉及离子的共存、物质鉴别、复分解反应、离子检验等,为高频考点,把握常见离子的反应及物质的性质为解答的关键,侧重基础知识的考查,题目难度不大.


科目:高中化学 来源: 题型:
天然水里一般含有Ca2+、Mg2+等多种离子。人们把含有较多量Ca2+、Mg2+的水叫做硬水,含有较少量或不含Ca2+、Mg2+的水叫做软水;降低水中
Ca2+、Mg2+含量的过程叫做硬水软化。如果硬度太高(含Ca2+、Mg2+的浓度太大)会给生产、生活带来很多不利,因此硬水的软化是水处理的重要方面之一。
离子交换法常用于工业锅炉用水的软化。离子交换剂多种多样,磺化煤(NaR)
就是一种阳离子交换剂。
(1)写出用磺化煤软化含Ca2+、Mg2+浓度较高的硬水的离子方程式________
__________________________________________________________________
_________________________________________________________________。
(2)用药剂软化法软化过的水总是含有一定浓度的Ca2+、Mg2+,其原因是
__________________________________________________________________
_________________________________________________________________。
(3)烧水后的锅炉或水壶中结有水垢,据此说明如果用硬度太高的水作锅炉用
水,主要的不利因素是_______________________________________________
_________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列描述正确的是()
A. 氯气、活性炭都能使品红溶液褪色,它们的漂白原理相同
B. 滴加石蕊试液显红色的溶液:Fe3+、NH4+、I﹣可能大量共存
C. 某溶液中加入盐酸酸化的氯化钡产生白色沉淀,原溶液中一定含有SO42﹣
D. Fe(N03)2溶液中滴加少量稀硫酸会变黄色
查看答案和解析>>
科目:高中化学 来源: 题型:
下列叙述正确的是()
A. 含有最低价元素的化合物不一定具有很强的还原性
B. 元素的单质一定是由氧化或还原该元素的化合物制得
C. 阳离子只能得电子被还原,阴离子只能失电子被氧化
D. 在化学反应中,得电子越多的氧化剂,其氧化性就越强
查看答案和解析>>
科目:高中化学 来源: 题型:
已知FeS2中铁元素的化合价为+2价,关于反应:4CuSO4+5FeS2+12H2O═7Cu2S+5FeSO4+12H2SO4的下列说法正确的是()
A. 该反应的氧化剂只有CuSO4
B. SO42﹣既不是氧化产物也不是还原产物
C. 1 mol CuSO4还原了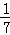 mol的S
mol的S
D. 被还原的S和被氧化的S的质量比为7:3
查看答案和解析>>
科目:高中化学 来源: 题型:
下列对化学知识概括合理的是()
A. 酸性氧化物都是非金属氧化物
B. 一种元素可能有多种氧化物,但同种化合价只对应一种氧化物
C. 丁达尔效应可用于区别溶液与胶体,云、雾均能产生丁达尔效应
D. 熔融状态能导电的物质一定是离子化合物
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是()
A. HClO中氯元素化合价比HClO4中氯元素化合价低,所以HClO4的氧化性强
B. 已知①Fe+Cu2+═Fe2++Cu;②2Fe3++Cu═2Fe2++Cu2+,则氧化性强弱顺序为:Fe3+>Cu2+>Fe2+
C. 已知还原性:B﹣>C﹣>D﹣,反应 2C﹣+D2═2D﹣+C2和反应2C﹣+B2═2B﹣+C2都能发生
D. 具有强氧化性和强还原性的物质放在一起就能发生氧化还原反应
查看答案和解析>>
科目:高中化学 来源: 题型:
2014年1月初华北地区连续5~6天出现大雾,致使高速公路封闭、飞机停飞.雾属于下列分散系中的()
A. 胶体 B. 悬浊液 C. 溶液 D. 乳浊液
查看答案和解析>>
科目:高中化学 来源: 题型:
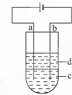
由于Fe(OH)2极易被氧化,所以实验室很难用亚铁盐溶液与烧碱反应制得白色纯净的Fe(OH)2沉淀.应用如下图所示电解实验可制得白色纯净的Fe(OH)2沉淀.两电极的材料分别为石墨和铁.
(1)a电极材料应为 ,电极反应式 ;
(2)电解液c可以是(填编号)
A.纯水 B.NaCl溶液 C.NaOH溶液 D.CuCl2溶液
(3)d为苯,其作用为 ,在加入苯之前对c应作怎样的简单处理? .
(4)为了在较短时间内看到白色沉淀,可采取的措施(填编号)
A.改用稀硫酸作电解液
B.适当增大电源的电压
C.适当减少两电极间距离
D.适当降低电解液的温度
(5)若c为Na2SO4溶液,当电解一段时间看到白色Fe(OH)2沉淀后,再反接电源电解,除了电极上看到气泡外,混合物中另一明显现象为 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com