
(6分)工业上常用铁质容器盛装冷浓硫酸。为研究铁质材料与热浓硫酸的反应,某学习小组进行了以下探究活动:
(1)将已去除表面氧化物的铁钉(碳素钢)放入冷浓硫酸中,10分钟后移入硫酸铜溶液中,片刻后取出观察,铁钉表面无明显变化,其原因是__________。
(2)另称取铁钉6.0 g放入15.0 mL浓硫酸中,加热,充分应后得到溶液X并收集到气体Y。
①甲同学认为X中除Fe3+外还可能含有Fe2+。若要确认其中的Fe2+,需进行的实验是__________。
②乙同学取336 mL(标准状况)气体Y通入足量溴水中,发生反应:
SO2+Br2+2H2O=2HBr+H2SO4
然后加入足量BaCl2溶液,经适当操作后得干燥固体2.33 g。由此推知气体Y中SO2的体积分数为(简要表述计算过程)__________。
(1)在冷浓硫酸中铁钉表面形成了一层致密的氧化物保护膜,阻止了铁与硫酸铜溶液的接触
(2)①向高锰酸钾酸性溶液中滴加溶液X,若紫红色褪去,则溶液X中含有Fe2+
②因为n(BaSO4)=0.01mol,根据硫原子守恒:n(BaSO4)=n(H2SO4)=n(SO2),n(SO2)=0.01mol,V(SO2)=2.24L,所以二氧化硫的体积分数为66.7%.
【解析】
试题分析:本题需将所学基础知识准确应用到解题过程,经过处理的铁钉放入冷浓硫酸中会发生钝化,再放入硫酸铜溶液时,不会出现明显变化;铁钉放入浓硫酸中加热时会发生反应,且开始生成Fe3+和SO2
气体,硫酸浓度逐渐变小,则会产生Fe2+和H2;若检验溶液中的Fe2+,须用酸性高锰酸钾溶液的氧化性;因为n(BaSO4)=0.01mol,根据硫原子守恒:n(BaSO4)=n(H2SO4)=n(SO2),n(SO2)=0.01mol,V(SO2)=2.24L,所以二氧化硫的体积分数为66.7%.
考点:金属铁与热浓硫酸反应的探究实验。


 暑假作业暑假快乐练西安出版社系列答案
暑假作业暑假快乐练西安出版社系列答案科目:高中化学 来源:2014-2015广东省揭阳市高二上学期期末考试化学文试卷(解析版) 题型:?????
化学与生活息息相关。下列说法正确的是
A.鲜榨橙汁遇到碘水会变蓝 B.馒头越嚼越甜
C.油脂经水解可以变成葡萄糖 D.土豆中的淀粉经水解可变成酒
查看答案和解析>>
科目:高中化学 来源:2014-2015广东省揭阳市高二上学期期末考试化学文试卷(解析版) 题型:?????
关于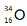 的叙述正确的是
的叙述正确的是
A.核电荷数为34 B.中子数为16
C.核外电子数为18 D.原子序数为16
查看答案和解析>>
科目:高中化学 来源:2014-2015广东省揭阳市高二上学期期末考试化学理试卷(解析版) 题型:选择题
下列说法正确的是
A.精炼铜时粗铜做阴极,纯铜做阳极
B.电解MgCl2饱和溶液,可制得金属镁
C.钢铁的腐蚀通常为电化学腐蚀,该腐蚀过程中负极反应为:Fe–3e-=== Fe 3+
D.氯碱工业和金属钠的冶炼都用到了NaCl,阳极反应都是:2C1一–2e- === C12↑
查看答案和解析>>
科目:高中化学 来源:2014-2015广东省揭阳市高二上学期期末考试化学理试卷(解析版) 题型:选择题
室温下,pH和体积均相同的盐酸和醋酸两份溶液,下列叙述正确的是
A.加适量的醋酸钠晶体后,两溶液的pH均增大
B.使温度都升高20 ℃后,两溶液的pH均不变
C.加水稀释2倍后,两溶液的pH均减小
D.加足量的锌粉充分反应后,两溶液中产生的氢气一样多
查看答案和解析>>
科目:高中化学 来源:2014-2015北京市东城区高一上学期期末考试化学试卷(解析版) 题型:实验题
(6分)实验室需要65 mL 1.0 mol/L的NaCl溶液用于测定AgNO3溶液的浓度。
(1)用NaCl固体配制NaCl溶液时必须用到的仪器是__________(填序号)。
①天平 ②烧杯 ③玻璃棒 ④酒精灯 ⑤胶头滴管 ⑥50 mL容量瓶 ⑦100 mL容量瓶
(2)需要称取NaCl固体的质量是__________。
(3)量取20 mL AgNO3溶液,当加入25 mL 1.0 mol/L NaCl溶液时恰好完全反应,则c(AgNO3)=____。
查看答案和解析>>
科目:高中化学 来源:2014-2015北京市东城区高一上学期期末考试化学试卷(解析版) 题型:选择题
下列说法不正确的是
A.标准状况下,11.2 L CO2的质量为22 g
B.0.1 mol Cl2与足量水反应转移电子0.2 mol
C.18 g H2O含有的原子总数为3×6.02×1023
D.0.5 mol/L Na2SO3溶液中Na+的物质的量浓度为1.0 mol/L
查看答案和解析>>
科目:高中化学 来源:2014-2015学年山西省高二12月月考化学试卷(解析版) 题型:填空题
(13分)(1)有人研究证明:使用氯气作自来水消毒剂,氯气会与水中有机物反应,生成如CHCl3等物质,这些物质可能是潜在的致癌致畸物质。目前人们已研发多种饮用水的新型消毒剂。下列物质不能作自来水消毒剂的是 (填序号)。
A.明矾 B.二氧化氯 C.臭氧 D.高铁酸钠(Na2FeO4)
(2)高铁(VI)酸盐是新一代水处理剂。其制备方法有:次氯酸盐氧化法(湿法)和高温过氧化物氧化法(干法)等。湿法是在碱性溶液中用次氯酸盐氧化铁(III)盐,写出该法的离子方程式: 。
(3)用高铁(VI)酸盐设计的高铁(VI)电池是一种新型可充电电池,电解质溶液为KOH溶液,放电时的总反应:3Zn+2K2FeO4+8H2O→3Zn(OH)2+2Fe(OH)3+4KOH
①写出正极发生的电极反应式: 。
②用高铁(VI)电池作电源,以Fe作阳极,以Cu作阴极,对足量KOH溶液进行电解,当有0.1molK2FeO4反应时,在电解池中生成H2 L(标准状况),同时生成Fe(OH)3= mol。
③下表列出了某厂排放的含锌废水中的含量及国家环保标准值的有关数据:
含锌废水水质 | 经处理后的水国家环保标准值 | |
Zn2+浓度/(mg·L-1) | ≤800 | ≤3.9 |
pH | 1~5 | 6~9 |
经处理后的废水pH=8,此时废水中Zn2+的浓度为 mg/L(常温下,Ksp[Zn(OH)2]=1.2×1017), (填“符合”或“不符合”)国家环保标准。
查看答案和解析>>
科目:高中化学 来源:2014-2015重庆市高一上学期第三次月考化学试卷(解析版) 题型:选择题
NA为阿伏加德罗常数,下列说法正确的是
A.1 mol Na2O和Na2O2混合物中含有的阴、阳离子总数是3NA
B.标准状况下,22.4 L NH3中含有电子数为8NA
C.1 mol Cl2与足量Fe反应转移电子数为3NA
D.1 mol·L-1的AlCl3溶液中, Cl-的数目为3NA
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com