
����Ŀ�����������;�㷺��
(1)��ҵ�ϳɰ��ķ�Ӧ�� N2+3H2![]() 2NH3 ��
2NH3 ��
�� һ���¶��£���ij500mL���ܱ������г���3mol H2 �� 1 mol N2��3min��Ӧ��ƽ�⣬H2�����ʵ���Ϊ0.75mol����
a. H2��ת���ʣ�_________
b.ƽ��ʱNH3���������______��(д���������)
�� ��������Ӧ������˵������ȷ����____________
A������Ӧ������淴Ӧ������ܽ��еĻ�ѧ��Ӧͳ��Ϊ���淴Ӧ
B�������淴Ӧ������Ӧ���ʺ��淴Ӧ�������ʱ���÷�Ӧ�ﵽ��ѧƽ��״̬
C����ѧ��Ӧ���Ⱦ����˷�Ӧ���ڸ������µ����ת����
D���ı���淴Ӧ�ķ�Ӧ����������һ���̶��ϸı��仯ѧƽ��״̬
(2)��֪�ճ����õĸɵ���У���缫�ֱ�Ϊ̼����пƤ���Ժ�״NH4Cl��ZnCl2��Ϊ����ʣ��缫��Ӧ�ɼ�Ϊ2NH4+ + 2e����2NH3+H2 (�����������MnO2����������H2����ˮ��NH3��Zn2+���Ϊ�ȶ�����)������������Ϣ���ճ����õĸɵ�ص�������__________��������_______������ʱ������_______������_______����������25.5��NH3ʱ��ת��______mol���ӡ�
���𰸡�75% 60% A ̼�� пƤ �� �� 1.5
��������
��1����������ʽ����Ӧ��ʽ���㣻
��2��ZnΪ������̼��Ϊ�ǽ�����ZnƤΪ������̼��Ϊ���������ԭ���ԭ������
��1��Ӧ������ʽ
N2+3H2![]() 2NH3
2NH3
��ʼ����mol�� 1 3 0
�仯����mol��0.75 2.25 1.5
ƽ������mol�� 0.25 0.75 1.5
(1) a. H2��ת����=![]() 100
100![]() 75%��
75%��
b.ƽ��ʱNH3���������=![]() 100
100![]() =60%��
=60%��
�� A.��ͬһ�����£�����Ӧ������淴Ӧ�������ͬʱ���еĻ�ѧ��Ӧͳ��Ϊ���淴Ӧ����A����
B�������淴Ӧ������Ӧ���ʺ��淴Ӧ�������ʱ���÷�Ӧ�ﵽ��ѧƽ��״̬����B��ȷ��
C����ѧ��Ӧ���Ⱦ����˷�Ӧ���ڸ������µ����ת���ʣ���C��ȷ��
D���ı���淴Ӧ�ķ�Ӧ����������һ���̶��ϸı��仯ѧƽ��״̬����D��ȷ��
�𰸣�A��
(2)�ɵ���нϻ��õĽ���п������,�ϲ����õĵ���ķǽ���̼���������ɵ�ع���ʱ������������̼�����·����п�������ɸ��������·����������������25.5��NH3ʱ������2NH4+ + 2e����2NH3+H2����֪ת�Ƶ������ʵ���=n��NH3��=![]() =1.5mol��
=1.5mol��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij��ɫ����Һ����ǿ���Ի������ܴ���������������ǣ� ��
A.Na+��SO42-��HCO3-��Cl��B.K+��Cl-��NO3-��Fe2+
C.Cu2+��Cl����NH4+��SO42-D.Mg2+��Cl����Na+��NO3-
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��(8��)��¯���������з�������Ҫ��ӦΪ
![]()
��֪�÷�Ӧ�ڲ�ͬ�¶��µ�ƽ�ⳣ�����£�

��ش��������⣺
(1)�÷�Ӧ��ƽ�ⳣ������ʽK=_____________����H________0(����>������<������=��)��
(2)��һ���ݻ�Ϊ10L���ܱ������У�1000��ʱ����Fe��Fe2O3��CO��CO2��1.0 mol����Ӧ����l0 min��ﵽƽ�⡣���ʱ�䷶Χ�ڷ�Ӧ��ƽ����Ӧ������(C02)= _____________��CO��ƽ��ת����= _____________��
(3)�����(2)��CO��ƽ��ת���ʣ��ɲ�ȡ�Ĵ�ʩ��_____________��
A������Fe���� | B������Fe203���� | C���Ƴ�����C02 |
D����߷�Ӧ�¶� E����С�������ݻ� F��������ʵĴ��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������£����и�������һ������ָ����Һ�д����������
A. pH=l ����Һ�У�Ba2+��Fe3+ ��Cl-��SCN-
B. ��ʹ��̪������Һ��Ca2+��K+��HCO3-��CO32-
C.  =10-12����Һ�У�NH4+��Cu2+��NO3-��SO42-
=10-12����Һ�У�NH4+��Cu2+��NO3-��SO42-
D. ��ˮ�����c(H+)=10-12mol��L-1����Һ�У�Na+��Al3+��Cl-��NO3-
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����һ���¶��£�10mL0.40mol/L H2O2�������ֽ⡣��ͬʱ�̲ⶨ����O2�������������Ϊ��״�������±���
t/min | 0 | 2 | 4 | 6 | 8 | 10 |
V(O2)/mL | 0.0 | 9.9 | 17.2 | 22.4 | 26.5 | 29.9 |
������������ȷ���ǣ���Һ����仯���Բ��ƣ�
A��0~6min��ƽ����Ӧ���ʣ�v��H2O2��![]()
![]() mol/(L��min)
mol/(L��min)
B��6~10min��ƽ����Ӧ���ʣ�v��H2O2����![]() mol/(L��min)
mol/(L��min)
C����Ӧ��6minʱ��c��H2O2��=0.3mol/L
D����Ӧ��6minʱ��H2O2�ֽ���50%
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij���淴Ӧ��2A(g)![]() B(g)+D(g)���ܱչ̶��ݻ���������4�ֲ�ͬ�����½��У�B��D����ʼŨ�Ⱦ�Ϊ0����Ӧ��A��Ũ���淴Ӧʱ��ı仯������±���
B(g)+D(g)���ܱչ̶��ݻ���������4�ֲ�ͬ�����½��У�B��D����ʼŨ�Ⱦ�Ϊ0����Ӧ��A��Ũ���淴Ӧʱ��ı仯������±���
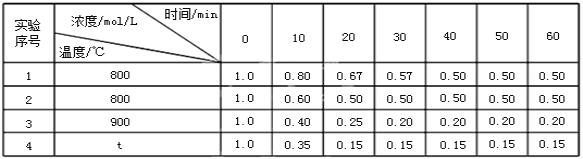
(1)ʵ��1�У���10��20min�ڣ�������A��ʾ��ƽ����Ӧ����Ϊ_____��
(2)0��20min�ڣ�ʵ��2��ʵ��1�ķ�Ӧ����(��������������)_____����ԭ�������_____��
(3)ʵ��3��ʵ��1�ķ�Ӧ����(����������������)_____����ԭ�������_____��
(4)�ӱ��п��Կ�����t_____900(������������������������)��
(5)ʵ��3��40����ʱ��(��)_____��(��)(������������������������)��
(6)ʵ��4��50����ʱB��Ũ��Ϊ_____��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��X��Y��Z�����ڱ������ڵ�����Ԫ�ء���֪X��Y��ͬ���壬Y��Zͬ���ڣ�����������ϵĵ�����֮��Ϊ16����������Ԫ�ؿ�����
A.Na��K��CaB.N��P��SC.N��P��SiD.F��Cl��S
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ߴ��Ⱦ�����ǵ��͵����ǽ����������ֳ����뵼�������������ķ��ֺ�ʹ��������������һ�� ���������������Ʊ���������ͼ��ʾ������˵����ȷ����
![]()
A. ����ٵĻ�ѧ����ʽΪ��SiO2��C![]() Si��CO2��
Si��CO2��
B. �������ڵ�Na2CO3���壬����ʯӢ����
C. ����������������ᷴӦ�����費��������ᷴӦ
D. SiHCl3���е�33.0�棩�к�������SiCl4���е�67.6�棩����ͨ����������ᴿSiHCl3
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������������ǵ�����������ء���֪��Ԫ�س����Ļ��ϼ���-2��0��+4��+6���֣��䲻ͬ��̬�����ʼ���ת�������������գ�
��1��д����������Ӧ�Ļ�ѧ����ʽ_____________________�����ò������ɫΪ_________��
��2��������������������������ڼ���ƿ�л�Ϸ�����Ӧ��������___________���������______��ѡ������������������ԭ��������
��3�������������γ��������Ԫ����֮һ���ɶ��������γɵ��������Ҫ�ɷ���_________��
��4�������ε�����ܶ࣬��Ӧ�ù㷺��ҽ���ϲ���____��X�����ӳ�θ���ڷ�ҩ����
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com