
【题目】向某密闭容器中充入 NO2,发生反应:2NO2(g) ![]() N2O4(g)。其它条件相同时,不同温度下平衡体系中各物质的物质的量分数如下表:(已知:N2O4 为无色气体)
N2O4(g)。其它条件相同时,不同温度下平衡体系中各物质的物质的量分数如下表:(已知:N2O4 为无色气体)
t/℃ | 27 | 35 | 49 | 70 |
NO2% | 20 | 25 | 40 | 66 |
N2O4% | 80 | 75 | 60 | 34 |
下列说法不正确的是
A.27℃时,该平衡体系中 NO2 的转化率为![]()
B.平衡时,NO2的消耗速率为N2O4消耗速率的2倍
C.室温时,将盛有NO2的密闭玻璃球放入冰水中其颜色会变浅
D.增大NO2起始量,可增大相同温度下该反应的化学平衡常数
科目:高中化学 来源: 题型:
【题目】8.34 g FeSO4·7H2O(相对分子质量:278)样品受热脱水过程的热重曲线(样品质量随温度变化的曲线)如下图所示,下列说法正确的是
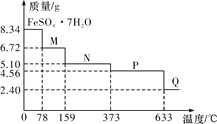
A. 温度为78 ℃时固体物质M的化学式为FeSO4·5H2O
B. 取适量380 ℃时所得的样品P,隔绝空气加热至650 ℃,得到一种固体物质Q,同时有两种无色气体生成,Q的化学式为Fe3O4
C. 在隔绝空气条件下,N得到P的化学方程式为FeSO4·H2O![]() FeSO4+H2O
FeSO4+H2O
D. 温度为159 ℃时固体N的化学式为FeSO4·2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】煤气化和液化是现代能源工业中重点考虑的能源综合利用方案。最常见的气化方法为用煤生产水煤气,而当前比较流行的液化方法为用煤生产CH3OH。
(1)已知:CO2(g)+3H2(g)=CH3OH(g)+H2O(g)△H1
2CO(g)+O2(g)=2CO2(g)△H2
2H2(g)+O2(g)=2H2O(g)△H3
则反应CO(g)+2H2(g)=CH3OH(g)的△H=_____。
(2)如图是该反应在不同温度下CO的转化率随时间变化的曲线。

①T1和T2温度下的平衡常数大小关系K1_____K2是不后填“>”、“<”或“=”)。
②由CO合成甲醇时,CO在250℃、300℃、350℃下达到平衡时转化率与压强的关系曲线如下图所示,则曲线c所表示的温度为_____℃。实际生产条件控制在250℃、1.3×104kPa左右,选择此压强的理由是_____。
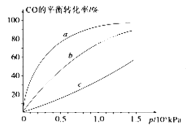
③以下有关该反应的说法正确的是_____(填序号)
A.恒温、恒容条件下,若容器内的压强不再发生变化,则可逆反应达到平衡
B.一定条件下,H2的消耗速率是CO的消耗速率的2倍时,可逆反应达到平衡。
C.使用合适的催化剂能缩短达到平衡的时间并提高CH3OH的产率。
D.某温度下,将2mo1CO和6molH2充入2L密闭容器中,充分反应,达到平衡后,测得c(CO)=0.2mol·L-1,则CO的转化率为80%
(3)一定温度下,向2L固定体积的密闭容器中加入1molCH3OH(g),发生反应:CH3OH(g)![]() CO(g)+2H2(g),H2的物质的量随时间变化的曲线如图所示。
CO(g)+2H2(g),H2的物质的量随时间变化的曲线如图所示。

0~2min内的平均反应速率v(CH3OH)=_____。该温度下,反应CO(g)+2H2(g)![]() CH3OH(g)的平衡常数K=_____。相同温度下,在一个恒容容器中加入一定量的CO和H2,发生反应2H2(g)+CO(g)=CH3OH(g)的平衡常数K=_____.相同温度下,若开始时加入CH3OH(g)的物质的量是原来的2倍,则____是原来的2倍。
CH3OH(g)的平衡常数K=_____。相同温度下,在一个恒容容器中加入一定量的CO和H2,发生反应2H2(g)+CO(g)=CH3OH(g)的平衡常数K=_____.相同温度下,若开始时加入CH3OH(g)的物质的量是原来的2倍,则____是原来的2倍。
A.平衡常数 B. CH3OH的平衡浓度 C.达到平衡的时间 D.平衡时气体的密度
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据下列实验操作和现象所得到的结论正确的是
选项 | 实验操作和现象 | 结论 |
A | 在0.1 molL-1Na2CO3溶液中,滴加2滴酚酞显浅红色,微热,红色加深 | CO32-水解是吸热反应 |
B | 等体积、pH=3的两种酸HA和HB分别与足量的Zn反应,酸HA放出的氢气多 | 酸性A比B强 |
C | 常温下,用饱和Na2CO3溶液可将BaSO4部分转化为BaCO3 | Ksp(BaSO4)>Ksp(BaCO3) |
D | 室温下,用pH试纸测得:0.1 molL-1 Na2SO3溶液的pH约为10;0.1 molL-1 NaHSO3溶液的pH约为5 | HSO |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】观察下列模型并结合有关信息,判断下列说法不正确的是( )
HCN | S8 | SF6 | B12结构单元 | |
结构模型 示意图 |
|
|
|
|
备注 | — | 易溶于CS2 | — | 熔点1 873 K |
A. HCN的结构式为H—C≡N,分子中含有2个σ键和2个π键
B. 固态硫S8属于原子晶体
C. SF6是由极性键构成的非极性分子
D. 单质硼属原子晶体,结构单元中含有30个B—B键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】亚铁氰化钾(K4[Fe(CN)6])双称黄血盐,是一种重要的化工原料。检验三价铁发生的反应为:K4[Fe(CN)6]+FeCl3=KFe[Fe(CN)6]↓(滕氏蓝) +3KCl,回答问题:
(1)写出基态Fe3+的核外电子排布式_________。
(2)K4[Fe(CN)6]中的作用力除共价键外,还有______和________。含有12mol σ键的K4[Fe(CN)6的物质的量为________mol。
(3)黄血盐中N原子的杂化方式为______;C、N、O的第一电离能由大到小的排序为_____,电负性由大到小的排序为________。
(4)Fe、Na、K的晶体结构如图所示:
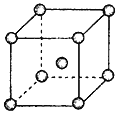
① 钠的熔点比钾更高,原因是__________________________。
② Fe原子半径是r cm,阿伏加德罗常数为NA,铁的相对原子质量为a,则铁单质的密度是_______g/cm3。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】生物浸出是用细菌等微生物从固体中浸出金属离子,有速率快、浸出率高等特点。氧化亚铁硫杆菌是一类在酸性环境中加速 Fe2+氧化的细菌,培养后能提供 Fe3+, 控制反应条件可达细菌的最大活性,其生物浸矿机理如下图。
![]()
反应1 反应2
(1)氧化亚铁硫杆菌生物浸出 ZnS 矿。
①反应 2 中有 S 单质生成,离子方程式是__。
② 实验表明温度较高或酸性过强时金属离子的浸出率均偏低,原因可能是__。
(2)氧化亚铁硫杆菌生物浸出废旧锂离子电池中钴酸锂(LiCoO2)与上述浸出机理相似,发生反应1 和反应3:LiCoO2 +3Fe3+=Li++ Co2++3Fe2++O2↑
①在酸性环境中,LiCoO2 浸出 Co2+的总反应的离子方程式是__。
②研究表明氧化亚铁硫杆菌存在时,Ag+对钴浸出率有影响,实验研究 Ag+的作用。取 LiCoO2 粉末和氧化亚铁硫杆菌溶液于锥形瓶中,分别加入不同浓度 Ag+的溶液,钴浸出率(图 1)和溶液 pH(图 2)随时间变化曲线如下:
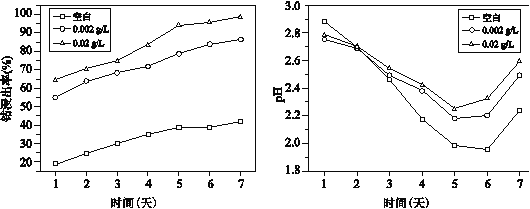
图1 不同浓度Ag+作用下钴浸出率变化曲线 图2 不同浓度Ag+作用下溶液中pH变化曲线
Ⅰ.由图 1 和其他实验可知,Ag+能催化浸出 Co2+,图 1 中的证据是__。
Ⅱ.Ag+是反应 3 的催化剂,催化过程可表示为: 反应 4:Ag++LiCoO2=AgCoO2+Li+
反应 5:……
反应 5 的离子方程式是__。
Ⅲ.由图 2 可知,第 3 天至第 7 天,加入 Ag+后的 pH 均比未加时大,结合反应解释其原因:__。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应中符合下列图像的是( )

A. N2(g)+3H2(g)![]() 2NH3(g) ΔH=-Q1kJ·mol-1(Q1>0)
2NH3(g) ΔH=-Q1kJ·mol-1(Q1>0)
B. 2SO3(g)![]() 2SO2(g)+O2(g) ΔH=+Q2kJ·mol-1(Q2>0)
2SO2(g)+O2(g) ΔH=+Q2kJ·mol-1(Q2>0)
C. 4NH3(g)+5O2(g)![]() 4NO(g)+6H2O(g) ΔH=-Q3kJ·mol-1(Q3>0)
4NO(g)+6H2O(g) ΔH=-Q3kJ·mol-1(Q3>0)
D. H2(g)+CO(g)![]() C(s)+H2O(g) ΔH=+Q4kJ·mol-1(Q4>0)
C(s)+H2O(g) ΔH=+Q4kJ·mol-1(Q4>0)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在体积固定的密闭容器中发生反应:![]() 。下列叙述中不能说明上述反应已达到化学平衡状态的是
。下列叙述中不能说明上述反应已达到化学平衡状态的是
A.混合气体的密度不变
B.体系的压强不变
C.混合气体的平均相对分子质量不变
D.反应体系中乙醇的物质的量浓度不再变化
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com