
| A. | 强电解质都易溶于水,所以BaSO4是弱电解质 | |
| B. | 一定条件下醋酸溶液的导电能力可能比稀硫酸强 | |
| C. | SO2的水溶液能导电,所以SO2是电解质 | |
| D. | 金刚石不导电,因此金刚石是非电解质 |
分析 电解质:在水溶液中或熔融状态下能导电的化合物;例:酸、碱、盐,金属氧化物等;
非电解质:在水溶液中和熔融状态下不能导电的化合物;例:有机物,非金属氧化物等;
能够完全电离的电解质为强电解质,只能部分电离的电解质为弱电解质;
电解质必须本身能够电离,据此判断解答.
解答 解:A.电解质强弱取决于电离程度,与溶解性无关,硫酸钡熔融状态下能够完全电离,属于强电解质,故A错误;
B.溶液导电能力强弱取决于自由移动离子浓度大小及离子带电荷多少,溶液的导电能力取决于溶液中离子浓度大小,与电解质的强弱无关,故醋酸溶液的导电能力可能比稀硫酸强,故B正确;
C.SO2的水溶液能导电是因为二氧化硫与水反应生成电解质亚硫酸,亚硫酸电离产生自由移动的离子,而二氧化硫本身不能电离,属于非电解质,故C错误;
D.电解质、非电解质必须都是化合物,金刚石为单质,既不是电解质,也不是非电解质,故D错误;
故选:B.
点评 本题考查简单的概念,明确电解质与非电解质都属于化合物,根据电离的程度来判断强弱电解质是解答的关键,题目难度不大.


 每日10分钟口算心算速算天天练系列答案
每日10分钟口算心算速算天天练系列答案科目:高中化学 来源: 题型:选择题
| A. | 锌粒与稀硫酸的反应 | |
| B. | 水分解生成氢气和氧气 | |
| C. | 甲烷在空气中燃烧的反应 | |
| D. | Ba(OH)2•8H2O晶体与NH4Cl晶体的反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 甲烷分子的球棍模型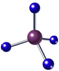 | |
| B. | Cl-的结构示意图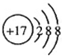 | |
| C. | 中子数为8的碳原子的核素符号为12C | |
| D. | 中子数为1的氢原子的核素符号为21H |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 都是银白色的柔软金属,密度都比水小 | |
| B. | 单质在空气中燃烧生成的都是过氧化物 | |
| C. | 碱金属单质都能与盐酸反应放出氢气 | |
| D. | 单质的熔、沸点随着原子序数的增加而升高 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | M一定是金属元素 | B. | M一定是S区元素 | C. | M的最高价是+1价 | D. | M可能呈现出-1价 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
| X | Y | Z | W | R | P | Q | |
| 原子半径/nm | 0.154 | 0.074 | 0.099 | 0.075 | 0.143 | ||
| 主要化合价 | -4,+4 | -2 | -1,+7 | -3,+5 | +3 | ||
| 其他 | 阳离子核外无电子 | 无机非金属材料的主角 | 焰色反应呈黄色 |
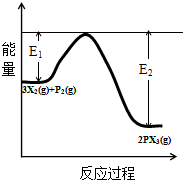
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
| 次数 | 第1次 | 第2次 |
| 加入稀盐酸的质量/g | 50 | 50 |
| 剩余固体的质量/g | 2.6 | 1 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com