

(1)0.1mol/L的CH3COOH、H2C2O4、H2SO3溶液pH最小的是____,最大的是___。
(2)KHSO3的溶液呈酸性,表明HSO3-的电离___水解(填“强于”、“弱手”或“等于”)。
(3)0.1mol/L的H2C2O4溶液与0.1mol/L NaOH溶液等体积混合,溶液的pH=a(溶液的体积等于混合前体积和)。
①则a___7(选填“>”、“<”、“=”或“不确定”);
②c(HC2O4-)+2c(C2O42-)=___(用含a的代数式表示)。
 学而优衔接教材南京大学出版社系列答案
学而优衔接教材南京大学出版社系列答案 小学课堂作业系列答案
小学课堂作业系列答案 金博士一点全通系列答案
金博士一点全通系列答案科目:高中化学 来源: 题型:阅读理解
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
查看答案和解析>>
科目:高中化学 来源:上海市十三校2012届高三第二次联考化学试题 题型:058
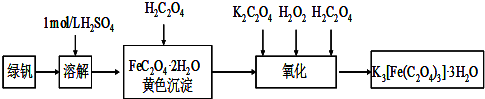
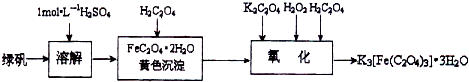
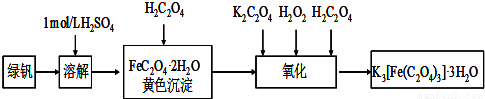
三草酸合铁(Ⅲ)酸钾晶体K3[Fe(C2O4)3]·3H2O可用于摄影和蓝色印刷.可用如下流程来制备.
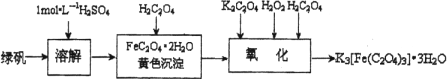
根据题意完成下列各题:
1.若用铁和稀硫酸制备FeSO4·7H2O________(填物质名称)往往要过量,理由是________.
2.要从溶液中得到绿矾,必须进行的实验操作是________.(按前后顺序填)
a.过滤洗涤
b.蒸发浓缩
c.冷却结晶
d.灼烧
e.干燥
某课外化学兴趣小组为测定三草酸合铁酸钾晶体(K3[Fe(C2O4)3]·3H2O)中铁元素含量,做了如下实验:
步骤一:称量5.000 g三草酸合铁酸钾晶体,配制成250 ml溶液.
步骤二:取所配溶液25.00 ml于锥形瓶中,加稀H2SO4酸化,滴加KMnO4溶液至草酸根恰好全部被氧化成二氧化碳,同时,MnO-4.被还原成Mn2+.向反应后的溶液中加入一定量锌粉,加热至黄色刚好消失,过滤,洗涤,将过滤及洗涤所得溶液收集到锥形瓶中,此时,溶液仍里酸性.
步骤三:用0.010 mol/L KMnO4溶液滴定步骤二所得溶液至终点,消耗KMnO4溶液20.02 ml,滴定中MnO4,被还原成Mn2+.
重复步骤二、步骤三操作,滴定消耗0.010 mol/L KMnO4溶液19.98 ml;
回答3-6小题:
3.配制三草酸合铁酸钾溶液需要使用的玻璃仪器除烧杯、玻璃棒以外还有________;主要操作步骤依次是:称量、________、转移、________、定容、摇匀.
4.加入锌粉的目的是________.
5.实验测得该晶体中铁的质量分数为________.在步骤二中,若加入的KMnO4的溶液的量不够,则测得的铁含量________.(选填“偏低”“偏高”“不变”)
6.某同学将8.74 g无水三草酸合铁酸钾(K3[Fe(C2O4)3])在一定条件下加热分解,所得固体的质量为5.42 g,同时得到密度为1.647 g/L(已折合成标准状况下)气体.研究固体产物得知,铁元素不可能以三价形式存在,而盐只有K2CO3.写出该分解反应的化学方程式________.
查看答案和解析>>
科目:高中化学 来源:2013-2014学年河北省高三第五次月考化学试卷(解析版) 题型:实验题
三草酸合铁(Ⅲ)酸钾晶体(K3[Fe(C2O4)3]·3H2O)有很重要的用途。可用如下流程来制备。根据题意完成下列各题:
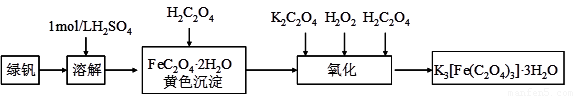
(1)要从溶液中得到绿矾,必须进行的实验操作是 。(按前后顺序填)
a.过滤洗涤 b.蒸发浓缩 c.冷却结晶 d.灼烧 e.干燥
某兴趣小组为测定三草酸合铁酸钾晶体(K3[Fe(C2O4)3]·3H2O)中铁元素含量,做了如下实验:
步骤1:称量5.000g三草酸合铁酸钾晶体,配制成250ml溶液。
步骤2:取所配溶液25.00ml于锥形瓶中,加稀H2SO4酸化,滴加KMnO4溶液至草酸根恰好全部被氧化成二氧化碳,同时,MnO4— 被还原成Mn2+。向反应后的溶液中加入一定量锌粉,加热至黄色刚好消失,过滤,洗涤,将过滤及洗涤所得溶液收集到锥形瓶中,此时,溶液仍里酸性。
步骤3:在酸性条件下,用0.010mol/L KMnO4溶液滴定步骤二所得溶液至终点,共做三次实验,平均消耗KMnO4溶液20.00ml,滴定中MnO4—,被还原成Mn2+。
(2)步骤1中,配制三草酸合铁酸钾溶液需要使用的玻璃仪器除烧杯、玻璃棒以外还有 ;
主要操作步骤依次是:称量、溶解、转移、 、定容、摇匀。
(3)步骤2中,加入锌粉的目的是 。
(4)步骤3中,发生反应的离子方程式为: 。
(5)步骤2中,若加入的KMnO4的溶液的量不够,则测得的铁含量 。(选填“偏低”、“偏高”、“不变”)
(6)某同学将8.74 g无水三草酸合铁酸钾(K3[Fe(C2O4)3])在一定条件下加热分解,所得固体的质量为5.42g,同时得到密度为1.647 g/L(已折合成标准状况下)气体(是物质的量之比为4:5的混合气体)。研究固体产物得知,铁元素不可能以三价形式存在,而盐只有K2CO3。写出该分解反应的化学方程式 。
查看答案和解析>>
科目:高中化学 来源:2012-2013学年江苏省常州一中高三(上)期中化学试卷(解析版) 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com