
| A. | 原子最外层电子数为2的元素一定处于周期表IIA族 | |
| B. | 元素周期表中位于金属和非金属分界线附近的元素属于过渡元素 | |
| C. | 某元素原子核外的电子数为63,则它是第6周期副族元素 | |
| D. | 除短周期外,其他周期均为18种元素,副族元素没有非金属元素 |
分析 A、原子最外层电子数为2的元素有He、第ⅡA族元素、第ⅡB族元素等;
B、元素周期表中位于金属和非金属分界线附近的元素属于半导体元素;
C、因核外电子数等于其质子数为63,用质子数分别减去各周期所含有的元素种类,63-2-8-8-18-18=9,显然其属于第六周期,从左到右的第9种;
D、第六周期有32种元素.
解答 解:A.原子最外层电子数为2的元素有He、第ⅡA族元素、第ⅡB族元素等,不一定为IIA族,故A错误;
B、元素周期表中位于金属和非金属分界线附近的元素属于半导体元素,而不是过渡元素,故B错误;
C、因核外电子数等于其质子数为63,用质子数分别减去各周期所含有的元素种类,63-2-8-8-18-18=9,显然其属于第六周期,从左到右的第9种,是副族元素,故C正确;
D、除短周期外,四、五周期均为18种元素,第六周期有32种元素,第七周期有26种元素,故D错误;
故选:C.
点评 本题考查元素周期表的结构与应用,为高频考点,把握元素的位置、周期中元素的种类、元素的性质等为解答的关键,侧重分析与应用能力的考查,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 124g P4含有的P-P键数为4NA(设NA表示阿伏伽德罗常数的值) | |
| B. | Be和NaOH溶液反应的离子方程式是:2Be+2OH -+2H2O=2BeO2-+3H2↑ | |
| C. | 在NaCl溶液中加入AgNO3溶液,生成白色沉淀;再加入氨水,沉淀消失,沉淀消失发生的离子方程式是: AgCl+2NH3•H2O=[Ag(NH3)2]++Cl-+2H2O | |
| D. | 0.1mol/L的Fe3+溶液中,能大量共存的离子有Cl-、SO42-、SCN- |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氢氧化钠的摩尔质量是40 g | |
| B. | 1 mol硫酸的质量是98g•mol-1 | |
| C. | 甲烷的摩尔质量就是它的相对分子质量 | |
| D. | 17 g NH3含N原子数是6.02×1023个 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
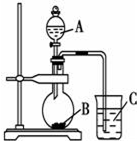 某研究性学习小组设计了一组实验验证元素周期律.
某研究性学习小组设计了一组实验验证元素周期律.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 汽车底盘喷涂油漆 | B. | 掺防腐的金属制成不锈钢菜刀 | ||
| C. | 地下钢管连接锌块 | D. | 钢闸门连接电源负极 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com