
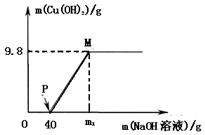
 向含CuCl2和HC1的100g混合溶液中,逐滴加入溶质质量分数为10%的NaOH溶液,参加反应的NaOH溶液质量与生成沉淀质量关系如图,仅考虑沉淀为Cu(OH)2则下列说法不正确的是( )
向含CuCl2和HC1的100g混合溶液中,逐滴加入溶质质量分数为10%的NaOH溶液,参加反应的NaOH溶液质量与生成沉淀质量关系如图,仅考虑沉淀为Cu(OH)2则下列说法不正确的是( )| A. | 整个反应过程中,氯离子个数不变 | |
| B. | M点溶液中的溶质有一种 | |
| C. | P点溶液比M点溶液中氯化钠的质量分数大 | |
| D. | 沉沉完全时,m1的数值为120 |
分析 A、根据复分解反应的实质来考虑;
B、M点表示氢氧化钠与盐酸和氯化铜恰好反应完,再分析溶质;
C、根据溶质质量和溶液质量的变化来分析;
D、根据沉淀质量算出与氯化铜反应的氢氧化钠的质量,再除以10%算出氢氧化钠溶液质量.
解答 解:A、复分解反应的实质是能生成气体、水、沉淀的离子参加了反应,即氢离子、氢氧根离子、铜离子参与反应,而氯离子实际并没有参加反应,所以整个反应过程中,氯离子个数不变,故A正确;
B、M点表示氢氧化钠与盐酸和氯化铜恰好反应完,盐酸和氢氧化钠反应生成了氯化钠和水,氢氧化钠和氯化铜反应生成氯化钠和氢氧化铜沉淀,故M点中的溶质是氯化钠,故B正确;
C、M点溶液比P点溶液中氯化钠的质量多了因为氢氧化钠与氯化铜反应生成了氯化钠,溶液质量少了,因为生成了沉淀,所以质量分数变大了,故C错误;
D、根据沉淀质量算出氢氧化钠质量为8克,所以需氢氧化钠溶液质量为80克,但这是与氯化铜反应需要的氢氧化钠,再加上与盐酸反应的氢氧化钠应该是120克,故D正确.
故选C.
点评 本题考查了复分解反应的实质,溶液质量分数的计算方法,并能依据图象分析所发生的化学反应是解题的关键,难度不大.


 天天练口算系列答案
天天练口算系列答案科目:高中化学 来源: 题型:推断题
 ,它的共价键属于极性(填“极性”或“非极性”)键;含有离子键和非极性共价键的化合物的电子式为
,它的共价键属于极性(填“极性”或“非极性”)键;含有离子键和非极性共价键的化合物的电子式为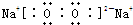 ;含有极性共价键和非极性共价键的化合物的电子式为
;含有极性共价键和非极性共价键的化合物的电子式为 .
. .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用 1体积的乙醇与 3体积的浓 H2SO4混合加热到 140℃制乙烯 | |
| B. | 加入适量浓溴水除去苯中混有的少量苯酚 | |
| C. | 用饱和食盐水和电石(CaC2)制乙炔 | |
| D. | 以盐酸、石灰石、苯酚钠溶液为试剂,验证酸性强弱关系:盐酸>石炭酸>碳酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 向溶液中加入硫酸酸化的NaCl溶液,生成白色沉淀,证明原溶液中含Ag+ | |
| B. | 向溶液中加入稀盐酸,生成使澄清石灰水变浑浊的无色无味气体,则原溶液中含CO32- | |
| C. | 向溶液中加入硝酸酸化的BaCl2溶液,生成白色沉淀,证明原溶液中含SO42- | |
| D. | 溶液中加入HCl酸化后,再加入BaCl2溶液,有白色沉淀产生,则溶液中含有SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1.5 g甲基(-CH3)所含电子数目为NA | |
| B. | 0.1 mol Mg在空气中完全燃烧生成MgO和Mg3N2,转移的电子数为0.2NA | |
| C. | 由2H和18O所组成的水11 g,其中所含的中子数为5NA | |
| D. | 1 mol Fe溶于过量硝酸,电子转移数为2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1 L该溶液中含溶质98 g | |
| B. | 从10 mL该溶液中取出5 mL后,剩余溶液的浓度不变 | |
| C. | 将4.9 g浓硫酸加入盛有50 mL蒸馏水的烧杯中充分溶解就可配得该浓度的硫酸溶液 | |
| D. | 该浓度的硫酸具有酸的通性 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在用蒸馏水洗涤烧杯时,洗液未全部注入容量瓶中 | |
| B. | 用量筒量取浓硫酸时,俯视刻度线 | |
| C. | 用来配制溶液的容量瓶用蒸馏水洗涤后未进行干燥处理 | |
| D. | 定容时俯视刻度线 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com