
资料:(1)草酸亚铁晶体(FeC2O4·2H2O)呈淡黄色;(2)KMnO4在酸性条件的还原产物为Mn2+。某课题组为探究草酸亚铁晶体的化学性质,进行了一系列实验探究。
(1)向盛有草酸亚铁晶体的试管中滴入几滴硫酸酸化的KMnO4溶液,振荡,发现溶液颜色逐渐变为棕黄色,并检测到CO2生成。这说明草酸亚铁晶体具有 (填“氧化性”、“还原性”或“碱性”)。若反应中消耗1 mol FeC2O4·2H2O,则参加反应的KMnO4为 ______mol。
(2)资料表明:在密闭容器中加热到一定温度时,草酸亚铁晶体可完全分解,生成几种氧化物,残留物为黑色固体。课题组根据课本上所介绍的铁的氧化物的性质,对黑色固体的组成提出如下假设,请你完成假设二和假设三:
假设一:全部是FeO;假设二: ;假设三:
(3)为验证上述假设一是否成立,课题组进行如下研究。
【定性研究】请你完成下表中内容。
|
实验步骤(不要求具体的操作过程) |
预期实验现象和结论 |
|
取少量黑色固体, |
|
【定量研究】课题组在文献中查阅到,FeC2O4·2H2O受热分解时,固体质量随温度变化的曲线如下图所示,写出加热到400℃时,FeC2O4·2H2O晶体受热分解的化学方程式为: 。
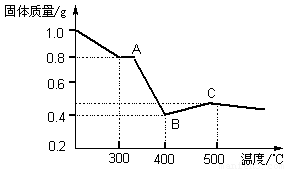
根据图象,如有1.0 g草酸亚铁晶体在坩埚中敞口充分加热,最终残留黑色固体的质量大于0.4 g。某同学由此得出结论:假设一不成立。你是否同意该同学的结论 (填“同意”或“不同意”),并简述理由 。
(共15分)
(1)还原性(1分),0.6(2分)
(2)假设二:全部是四氧化三铁(2分);假设三:氧化亚铁和四氧化三铁的混合物(2分)
(3)[定性研究] 实验步聚:取少量黑色固体,加入适量的稀盐酸(或稀硫酸)溶解(1分),在溶液中加入KSCN溶液(1分)。现象与结论:若溶液不变红,则假设一成立(1分),若溶液变红,则假设一不成立(1分)。
[定量研究]FeC2O4.2H2O FeO+CO+CO2+2H2O(2分,或FeC2O4
FeO+CO+CO2+2H2O(2分,或FeC2O4  FeO+CO+CO2)
FeO+CO+CO2)
不同意(1分),实验未在密闭容器中进行,FeO会被空气进一步氧化,生成铁的其它氧化物(1分)。
【解析】
试题分析:
(1)结合题中信息可以得出草酸亚铁晶体具有还原性;利用电子守恒1 mol FeC2O4·2H2O中+2价Fe和+3价C分别被氧化为+3价和+4价,所以1 mol FeC2O4·2H2O共失去3mole-,KMnO4在酸性条件的还原产物为Mn2+,1mol KMnO4得到5mol e-,则参加反应的KMnO4为0.6mol。
(2)黑色的铁的氧化物有氧化亚铁和四氧化三铁两种; 根据Fe2+不能使KSCN溶液变红, Fe3+能使KSCN溶液变红,得出定性研究实验步聚、现象与结论。
(3)定量研究中,m(FeC2O4·2H2O)=1g, 则n(FeC2O4·2H2O)=1/180mol,FeC2O4·2H2O中H2O的质量分数为1/5,结合图像加热到200℃时间内,是失去水的过程;200℃-400℃时,若C全部转化为CO2,则△m=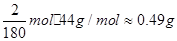 ;若C全部转化为CO,△m=
;若C全部转化为CO,△m=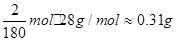 ,实际△m=0.4g,设n(CO2)=xmol,n(CO)=2/180
– xmol。解得x=1/180,所以产物为n(CO2)/
n(CO)=1/1的混合气体可得:FeC2O4.2H2O
,实际△m=0.4g,设n(CO2)=xmol,n(CO)=2/180
– xmol。解得x=1/180,所以产物为n(CO2)/
n(CO)=1/1的混合气体可得:FeC2O4.2H2O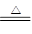 FeO+CO+CO2+2H2O或FeC2O4
FeO+CO+CO2+2H2O或FeC2O4 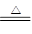 FeO+CO+CO2;实验未在密闭容器中进行,FeO会被空气进一步氧化,生成铁的其它氧化物,而使残留物质量变化。
FeO+CO+CO2;实验未在密闭容器中进行,FeO会被空气进一步氧化,生成铁的其它氧化物,而使残留物质量变化。
考点:本题以探究实验为基础,考查了元素及化合物性质、探究基本方法,氧化还原反应计算,结合图像的化学计算。


 天天向上口算本系列答案
天天向上口算本系列答案科目:高中化学 来源: 题型:阅读理解

 这样便得到了高纯度的纳米铁粉.
这样便得到了高纯度的纳米铁粉.
| ||
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
| ||

| ||
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
| 实验步骤(不要求具体的操作过程) | 预期实验现象和结论 |
| 取少量黑色固体, |
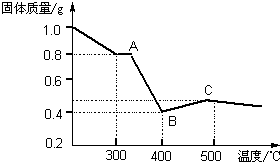 [定量研究]课题组在文献中查阅到,FeC2O4?2H2O受热分解时,固体质量随温度变化的曲线如图所示,写出加热到400℃时,FeC2O4?2H2O晶体受热分解的化学方程式为:
[定量研究]课题组在文献中查阅到,FeC2O4?2H2O受热分解时,固体质量随温度变化的曲线如图所示,写出加热到400℃时,FeC2O4?2H2O晶体受热分解的化学方程式为:查看答案和解析>>
科目:高中化学 来源:2012-2013学年安徽省高三年级第一次联考理综化学试卷(解析版) 题型:实验题
草酸亚铁晶体(FeC2O4·2H2O)呈淡黄色。某课题组为探究草酸业铁晶体的化学性质, 进行了一系列实验探究。
(1)向盛有草酸亚铁晶体的试管中滴入几滴硫酸酸化的KMnO4溶液,振荡,发现溶液颜色逐渐变为棕黄色,并检测到二氧化碳气体生成。这说明草酸亚铁晶体具有 (填“氧化性”、“还原性”或“碱性”)。若反应中消耗1 mol FeC2O4·2H2O,则参加反应的KMnO4为 mol。
(2)资料表明:在密闭容器中加热到一定温度时,草酸亚铁晶体可完全分解,生成几种氧化物,残留物为黑色固体。课题组根据课本上所介绍的铁的氧化物的性质,对黑色固体的组成提出如下假设,请你完成假设二和假设三:
假设一:全部是FeO
假设二:
假设三:
(3)为验证上述假设一是否成立,课题组进行如下研究。
【定性研究】请你完成下表中内容。
|
实验步骤(不要求写出具体操作过程) |
预期实验现象和结论 |
|
取少量黑色固体,
|
|
【定量研究】课题组在文献中查阅到,FeC2O4·2H2O受热分解时,固体质量随温度变化的曲线如下图所示,写出加热到400℃时,FeC2O4·2H2O晶体受热分解的化学方程式为: 。

根据图象,如有1.0 g草酸亚铁晶体在坩埚中敞口充分加热,最终残留黑色固体的质量大于0.4 g。某同学由此得出结论:假设一不成立。你是否同意该同学的结论,并简述理由:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com