
元素 | Na | Mg | Al | Si | P | S | |
与水反应的条件、程度及方程式 |
|
|
|
|
|
| |
气态氢化物 | 化学式 | — |
|
|
| ||
与H2反应的条件、程度 | — |
|
|
| |||
氢化物的稳定性 | — |
|
|
| |||
最高价氧化物对应水化物 | 化学式 |
|
|
|
|
|
|
酸碱性 |
|
|
|
|
|
| |
电解质的类别 |
|
|
|
|
|
| |
酸碱性的变化规律 |
|
|
|
|
|
| |
元素 | Na | Mg | Al | Si | P | S | Cl | |
与水反应的条件、程度及方程式 | 冷水剧烈2Na+2H2O
| 沸水较缓Mg+2H2O
| 沸水 很慢 | — | — | — | 与水缓慢反应,但不放H2Cl2+H2O
HClO | |
气态氢化物 | 化学式 | — |
| SiH4 | PH3 | H2S | HCl | |
与H2反应的条件、程度 | — |
| 高温(常用间接法) | 磷蒸气与H2反应 | 加热 | 点燃或光照 | ||
氢化物的稳定性 | — |
| 爆炸性自燃 | 自燃 | 很稳定 | |||
最高价氧化物对应水化物 | 化学式 | NaOH | Mg(OH)2 | Al(OH)3 (H3AlO3) | H4SiO4(H2SiO3) | H3PO4 | H2SO4 | HClO4 |
酸碱性 | 强碱 | 中强碱 | 两性 | 弱酸 | 中强酸 | 强酸 | 最强酸 | |
电解质的类别 | 强 | 弱 | 弱 | 弱 | 弱 | 强 | 强 | |
酸碱性的变化规律 |
| |||||||


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
| 元素 | 甲 | 乙 | 丙 |
| 元素符号 | ① Na Na |
② Cl Cl |
O |
| 原子结构示意图 | 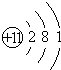 |
③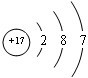  |
④  |
| 周期 | 三 | 三 | ⑤ 二 二 |
| 族 | ⑥ IA IA |
ⅦA | ⑦ VIA VIA |
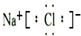
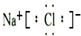
查看答案和解析>>
科目:高中化学 来源: 题型:
| 元素 | 甲 | 乙 | 丙 |
| 元素符号 | ① Na Na |
② Cl Cl |
0 |
| 原子结构示意图 | 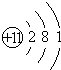 |
③  |
④  |
| 周期 | 三 | 三 | ⑤ 二 二 |
| 族 | ⑥ ⅠA ⅠA |
ⅦA | ⑦ ⅥA ⅥA |
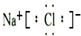
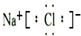
查看答案和解析>>
科目:高中化学 来源: 题型:
| 1 |
| 2 |
| 实验序号 | 起始浓度/mol?L-1 | R2平衡转化率 | |
| c(XZ2) | c(R2) | ||
| ① | 1.5 | 1.0 | 60% |
| ② | 3.0 | 1.0 | |
查看答案和解析>>
科目:高中化学 来源: 题型:
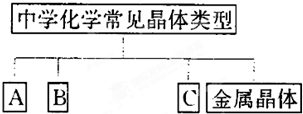
| A | B | C | ||
| 晶体类别 | 金属晶体 | |||
| 实例的化学式 | Na |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com