
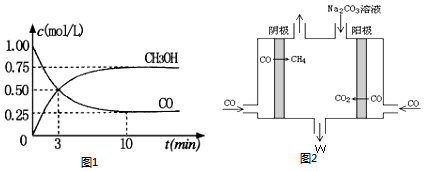
分析 (1)利用盖斯定律计算反应热,得到平衡状态时,正逆反应速率相等,各物质的浓度不变,由此衍生的一些物理量也不变;
(2)①根据v=$\frac{△c}{△t}$,计算甲醇的反应速率,反应速率之比等于化学方程式计量数之比计算氢气的反应速率,化学平衡常数为生成物浓度幂之比与反应物浓度幂之积的比进而求得化学平衡常数,计算再充入1molCO(g)和1molCH3OH(g)的浓度商和平衡常数比较平淡反应进行的方向;
②由此电解原理可知,阳极失去电子生成二氧化碳气体,加入碳酸钠,碳酸钠与二氧化碳反应生成碳酸氢钠,阴极CO得到电子生成甲烷气体,甲醇燃料电池,甲醇在负极失电子发生氧化反应,氧气在正极放电,酸性条件下生成水;
(3)(NH4)2SO4为强酸弱碱盐,NH4+水解显酸性,根据电荷守恒:c(NH4+)+c(Na+)+c(H+)=2c(SO42-)+c(OH-),由物料守恒可知c(NH4+)+c(NH3•H2O)=2c(SO42-),结合溶液呈中性,联立判断.
解答 解:(1)2SO2(g)+O2(g)?2SO3(g)△H=-196.6kJ•mol-1①
2NO(g)+O2(g)?2NO2(g)△H=-113.0kJ•mol-1 ②
将方程式$\frac{①-②}{2}$得:NO2(g)+SO2(g)?SO3(g)+NO(g)△H=$\frac{-196.6KJ/mol-(-113.0KJ/mol)}{2}$=-41.8kJ/mol,
a.随反应:NO2(g)+SO2(g)?SO3(g)+NO(g)的进行,气体的质量和体积都不变,所以ρ=$\frac{m}{V}$也不变,不能说明到达平衡状态,故a错误;
b.混合气体颜色保持不变,说明二氧化氮的浓度不变,说明到达平衡状态,故b正确;
c.随反应进行,SO3和NO都是生成物,所以体积比一直等于系数比,所以SO3和NO的体积比保持不变,不能说明到达平衡状态,故c错误;
d.反应速率之比等于化学方程式计量数之比为正反应速率之比,ν(NO2):ν(SO2):ν(SO3):ν(NO)=1:1:1:1,反应自始至终都按此比例进行,故d错误;
故答案为:-41.8; b;
(2)图象分析可知,甲醇变化浓度为0.75mol/L,甲醇的反应速率v(CH3OH)=$\frac{0.75mol/L}{10min}$=0.075mol/(L•min ),反应速率之比等于化学方程式计量数之比,v(H2)=v(CH3OH)=2×0.075mol/(L•min )=0.15mol/(L•min ),
结合化学三行计算得到,图象分析可知体积为1L,
CO+2H2?CH3OH
起始量(mol/L) 1 2 0
变化量(mol/L) 0.75 1.5 0.75
平衡量(mol/L) 0.25 0.5 0.75
K=$\frac{0.75}{0.25×0.{5}^{2}}$=12
第10min后,保持温度不变,向该密闭容器中再充入1molCO(g)和1molCH3OH(g),
Qc=$\frac{1.75}{1.25×0.{5}^{2}}$=5.6<K=12,平衡正向进行,
故答案为:0.15;
②由此电解原理可知,阳极失去电子生成二氧化碳气体,加入碳酸钠,碳酸钠与二氧化碳反应生成碳酸氢钠,阴极CO得到电子生成甲烷气体,据此离子反应方程式为:4CO+3CO32-+5H2O=6HCO3-+CH4↑,阴极区电极反应式为:CO+6e-+5H2O=6OH-+CH4,甲醇燃料电池酸性条件下该燃料电池的正极反应式为O2+4e-+4H+=2H2O,电池负极反应式为:CH3OH+H2O-6e-═CO2+6H+,生成标准状况下1.12LCH4物质的量=$\frac{1.12L}{22.4L/mol}$=0.05mol
电子守恒得到CH4~CH3OH~6e-,
需要消耗CH3OH的质量=0.05mol×32g/mol=1.6g,
故答案为:CO+6e-+5H2O=6OH-+CH4;1.6;
(3)(NH4)2SO4为强酸弱碱盐,NH4+水解显酸性:NH4++H2O?NH3•H2O+H+,室温时,向(NH4)2SO4溶液中滴入NaOH溶液至溶液呈中性,根据电荷守恒:c(NH4+)+c(Na+)+c(H+)=2c(SO42-)+c(OH-),溶液呈中性,而c(H+)=c(OH-),故c(NH4+)+c(Na+)=2c(SO42-),由物料守恒可知c(NH4+)+c(NH3•H2O)=2c(SO42-),联立可得c(Na+)=c(NH3•H2O),则所得溶液中微粒浓度大小关系c(Na+)=c(NH3•H2O),
故答案为:NH4++H2O?NH3•H2O+H+;=.
点评 本题考查了盖斯定律的应用、平衡状态的判断、平衡常数的计算、氧化还原反应化学方程式的书写及其计算、图象的分析与应用等,考查了学生的分析能力以及对基础知识的综合应用能力,题目难度中等.


 仁爱英语同步练习册系列答案
仁爱英语同步练习册系列答案 学习实践园地系列答案
学习实践园地系列答案科目:高中化学 来源: 题型:选择题
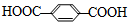 +nHOCH2CH2OH$\stackrel{一定条件}{→}$涤纶+(2n-1)H2O下列说法正确的是( )
+nHOCH2CH2OH$\stackrel{一定条件}{→}$涤纶+(2n-1)H2O下列说法正确的是( )| A. | 合成涤纶的反应为加聚反应 | |
| B. | 对苯二甲酸和苯甲酸互为同系物 | |
| C. | 1 mol涤纶与NaOH溶液反应,理论上最多可消耗2n mol NaOH | |
| D. | 涤纶的结构简式为: |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 钠与CuSO4溶液反应:2Na+Cu2+═Cu+2Na+ | |
| B. | 稀H2SO4和Ba(OH)2溶液反应:H++SO42-+Ba2++OH-═BaSO4+H2O | |
| C. | 少量SO2通入苯酚钠溶液中:C6H5O-+SO2+H2O═2C6H5OH+SO32- | |
| D. | 醋酸钠的水解反应:CH3COO-+H3O+═CH3COOH+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
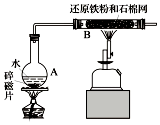 某校化学小组学生利用如图所列装置进行“铁与水反应”的实验.(图中夹持及尾气处理装置均已略去)
某校化学小组学生利用如图所列装置进行“铁与水反应”的实验.(图中夹持及尾气处理装置均已略去)查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 配制0.1mol/LNaCl溶液,定容时不小心加水超过刻度线,立即将水吸出 | |
| B. | 实验室制取氧气并用排水法收集,出现倒吸现象,立即停止加热 | |
| C. | 少量浓硫酸沾在皮肤上,立即用大量水冲洗,并涂上稀NaOH溶液 | |
| D. | 使用分液漏斗萃取碘水中的碘,振荡过程中要适时打开活塞进行“放气” |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
 ;A与C组成的化合物为MgS(用具体元素符号表示).
;A与C组成的化合物为MgS(用具体元素符号表示).查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com