
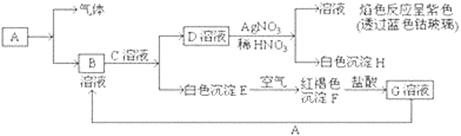
 Fe3O4+4H2
Fe3O4+4H2  Fe3O4+4H2
Fe3O4+4H2 

科目:高中化学 来源:不详 题型:单选题
| A.熔点比生铁的低 |
| B.与相同浓度的盐酸反应生成氢气的速率比生铁的快 |
| C.在冷的浓硫酸中可以钝化 |
| D.在潮湿空气中比生铁容易被腐蚀 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
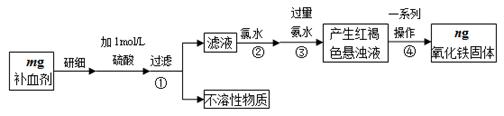
| A.KSCN溶液 | B.酸性KMnO4溶液 | C.铁粉 | D.FeCl3溶液 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| 物质(25℃) | Cu(OH)2 | Fe(OH)2 | Fe(OH)3 |
| Ksp | 2.2×10-20 | 8.0×10-16 | 4.0×10-38 |
| 完全沉淀时的pH | ≥6.4 | ≥9.6 | 3~4 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
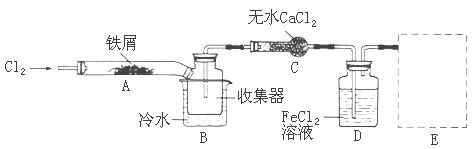
| A.氢氧化钠溶液 | B.酸性高锰酸钾溶液 | C.硫氰化钾溶液 | D.氨水 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.5.6 g | B.11.2 g | C.22.4 g | D.33.6 g |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 2Cu + SO2
2Cu + SO2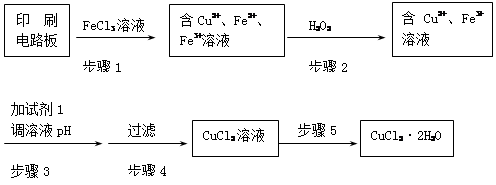
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.2∶3 | B.3∶2 | C.1∶2 | D.1∶1 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.只含Cu2+、Fe2+、Zn2+ | B.只含Zn2+ |
| C.只含Fe2+、Zn2+ | D.只含Cu2+、Fe3+、Zn2+ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com