
如图:横坐标为溶液的pH,纵坐标为Zn2+或[Zn(OH)4]2-物质的量浓度的对数,回答下列问题。
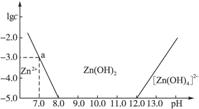
(1)往ZnCl2溶液中加入足量的氢氧化钠溶液,反应的离子方程式可表示为____________。
(2)从图中数据计算可得Zn(OH)2的溶度积Ksp=____________。
(3)某废液中含Zn2+,为提取Zn2+可以控制溶液pH的范围是____________。
 励耘书业暑假衔接宁波出版社系列答案
励耘书业暑假衔接宁波出版社系列答案科目:高中化学 来源: 题型:阅读理解
 (2011?惠州模拟)铁、铜都是人类最早使用的金属,它们的单质及化合物应用非常广泛.
(2011?惠州模拟)铁、铜都是人类最早使用的金属,它们的单质及化合物应用非常广泛.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
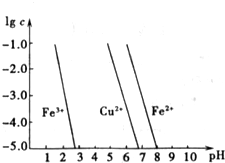 铁、铜都是人类最早使用的金属,它们的单质及化合物应用非常广泛.
铁、铜都是人类最早使用的金属,它们的单质及化合物应用非常广泛.查看答案和解析>>
科目:高中化学 来源: 题型:
(10分)如图横坐标为溶液的pH值,纵坐标为Zn2+ 离子或Zn(OH)42-离子(配离子)物质的量浓度的对数,回答下列问题.

(1)往ZnCl2溶液中加入足量的氢氧化钠溶液,反应的离子方程式可表示为 。
(2)从图中数据计算可得Zn(OH)2的溶度积(Ksp)= 。
(3)某废液中含Zn2+ 离子,为提取Zn2+ 离子可以控制溶液中pH值的范围是 。
(4)往1L 1.00 mol?L-1 ZnCl2溶液中加入NaOH固体至pH=6,需NaOH mol (精确到小数点后2位)。
(5)25℃时,PbCl2固体在盐酸中的溶解度如下:
c(HCl)/ (mol?L-1) | 0.50 | 1.00 | 2.04 | 2.90 | 4.02 | 5.16 | 5.78 |
103 c(PbCl2)/ (mol?L-1) | 5.10 | 4.91 | 5.21 | 5.90 | 7.48 | 10.81 | 14.01 |
根据上表数据判断下列说法正确的是 。
![]() A.随着盐酸浓度的增大,PbCl2固体的溶解度先变小后又变大
A.随着盐酸浓度的增大,PbCl2固体的溶解度先变小后又变大
![]() B.PbCl2固体在0.50 mol?L-1盐酸中的溶解度小于在纯水中的溶解度
B.PbCl2固体在0.50 mol?L-1盐酸中的溶解度小于在纯水中的溶解度
![]() C.PbCl2能与浓盐酸反应生成一种难电离的阴离子(配离子)
C.PbCl2能与浓盐酸反应生成一种难电离的阴离子(配离子)
![]() D.PbCl2固体可溶于饱和食盐水
D.PbCl2固体可溶于饱和食盐水
查看答案和解析>>
科目:高中化学 来源:2011年广东省惠州市高考化学模拟试卷(解析版) 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com