
| 选项 | 实验目的 | 实验方案 |
| A | 证明其他条件不变时,增大反应物浓度,反应速率加快 | 常温下,对比等量铝粉分别与稀硫酸反应的反应速率 |
| B | 证明SO2具有氧化性 | 将SO2通入酸性KMnO4溶液中,观察溶液是否褪色 |
| C | 证明Ksp(AgCl)>Ksp(Ag2S) | 向2mL0.1mol•L-1AgNO3溶液中加入1mL0.1mol•L-1NaCl溶液,出现白色沉淀,再加入几滴0.1mol•L-1的Na2S溶液,有黑色沉淀生成 |
| D | 证明“84”消毒液(含NaClO)的氧化能力随溶液pH减小而增强 | 将“84”消毒液滴入品红溶液中,褪色缓慢,若同时加入食醋,红色很快退去 |
| A. | A | B. | B | C. | C | D. | D |
分析 A.稀硫酸浓度不同,反应速率不同;
B.二氧化硫具有还原性,与高锰酸钾发生氧化还原反应;
C.硝酸银过量,不能比较溶度积大小;
D.加入醋酸,溶液酸性增强,红色很快褪去,可证明实验结论.
解答 解:A.稀硫酸浓度不同,反应速率不同,浓度越大,反应速率越大,可通过实验证明,故A正确;
B.二氧化硫具有还原性,与高锰酸钾发生氧化还原反应,如证明二氧化硫的氧化性,可与硫化钠溶液反应,看是否生成沉淀,故B错误;
C.硝酸银过量,两种沉淀都生成,不存在沉淀的转化问题,不能比较溶度积大小,故C错误;
D.加入醋酸,溶液酸性增强,红色很快褪去,可证明实验结论,故D正确.
故选AD.
点评 本题考查化学实验方案评价,为高频考点,涉及反应速率影响因素、性质比较、难溶电解质的溶解平衡等知识点,明确实验原理、物质性质是解本题关键,同时还考查学生分析判断及比较能力,易错选项是C.


 快乐小博士巩固与提高系列答案
快乐小博士巩固与提高系列答案科目:高中化学 来源: 题型:选择题
| A. | 将铜片放入浓硫酸中,无明显实验现象,说明铜在冷的浓硫酸中发生钝化 | |
| B. | 油脂制肥皂实验中加乙醇的目的是增大油脂的溶解度从而加快油脂皂化反应速率 | |
| C. | 工业合成氨的反应属于能自发进行的反应,故能迅速发生 | |
| D. | 鸡蛋清溶液中加入饱和Na2SO4溶液有沉淀生成是因为蛋白质变性 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
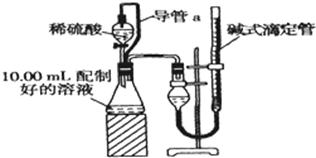 实验室测定碳酸钠和碳酸氢钠混合物中碳酸钠的质量分数W(Na2CO3),称取此混合物5.0g,溶于水中,配成250mL溶液.
实验室测定碳酸钠和碳酸氢钠混合物中碳酸钠的质量分数W(Na2CO3),称取此混合物5.0g,溶于水中,配成250mL溶液.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
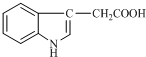 1934年,科学家首先从人尿中分离出具有生长素效应的化学物质--吲哚乙酸,吲哚乙酸的结构如图所示.下列有关吲哚乙酸的说法中正确的是( )
1934年,科学家首先从人尿中分离出具有生长素效应的化学物质--吲哚乙酸,吲哚乙酸的结构如图所示.下列有关吲哚乙酸的说法中正确的是( )| A. | 吲哚乙酸与苯丙氨酸互为同分异构体 | |
| B. | 1 mol吲哚乙酸与足量氢气发生加成反应时,可以消耗5 mol H2 | |
| C. | 吲哚乙酸苯环上的二氯代物共有四种结构 | |
| D. | 吲哚乙酸可以发生取代反应、加成反应、氧化反应和还原反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 实验 | 现象 | 结论 | |
| A | 将饱和食盐水滴入工业电石得到的气体通入酸性KMnO4溶液中 | KMnO4溶液紫红色褪去 | 证明生成了乙炔气体 |
| B | 将BaSO4与浓Na2CO3溶液混合后振荡静置,过滤并洗净所得的沉淀,往滴加足量盐酸 | 产生使澄清石灰水变浑浊的气体 | Ksp(BaCO3)<Ksp(BaSO4) |
| C | 充分加热花生油与NaOH混合溶液(已加沸石) | 溶液不再分层 | 花生油的水解反应已经趋于完全 |
| D | 向含KSCN的FeI2溶液中滴加足量氯水 | 溶液变为血红色 | 还原性:Fe2+>I- |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
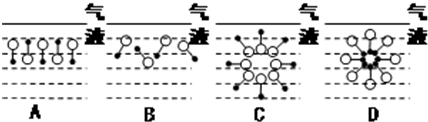
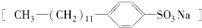 是常用洗涤剂的主要成分.其结构可用图形
是常用洗涤剂的主要成分.其结构可用图形 来表示,•端为链烃基,O端为极性基.根据这一结构特点,试分析和回答下列问题:
来表示,•端为链烃基,O端为极性基.根据这一结构特点,试分析和回答下列问题: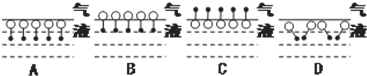
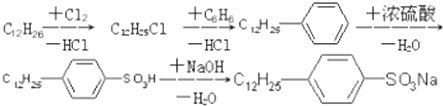
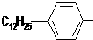 .
.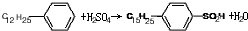 ,反应类型为取代反应.
,反应类型为取代反应.查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | Ba2Cl2、CuSO4、NaOH、NaCl | B. | Na2SO4、BaCl2、K2CO3、KNO3 | ||
| C. | FeCl3、NaOH、Na2SO4、Ba(NO3)2 | D. | NaCl、Na2CO3、Ca(NO3)2、H2SO4 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用长颈漏斗分离出乙酸与乙醇反应的产物 | |
| B. | 用向上排空气法收集铜粉与稀硝酸反应产生的NO | |
| C. | 配制氯化铁溶液时,将氯化铁溶解在较浓的盐酸中再加水稀释 | |
| D. | 将Cl2与HCl混合气体通过饱和食盐水可得到纯净的Cl2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com