
分析 (1)根据三段式解题法,求出反应混合物各组分浓度的变化量、平衡时各组分的浓度,代入平衡常数表达式计算平衡常数;
(2)计算常数的浓度商Qc、平衡常数,与平衡常数比较判断反应进行方向.
解答 解:(1)平衡时CO的转化率为60%,则CO的浓度变化量=2mol/L×60%=1.2mol/L,则:
CO(g)+H2O(g) ?CO2(g)+H2(g)
?CO2(g)+H2(g)
起始(mol/L):2 3 0 0
变化(mol/L):1.2 1.2 1.2 1.2
平衡(mol/L):0.8 1.8 1.2 1.2
故平衡常数K=$\frac{1.2×1.2}{0.8×1.8}$=1,
用H2O表示的化学反应速率为$\frac{1.2mol/L}{4s}$=0.3mol•L-1•s-1,
故答案为:1;
(2)在相同温度下(850℃),若起始时c(H2O)=2mol•L-1,c(CO)=c(CO2)=1mol•L-1,c(H2)=1.5mol•L-1,则根据反应 CO(g)+H2O(g)═CO2(g)+H2 (g)有浓度商Qc=$\frac{1×1.5}{2×1}$=0.75<1,故平衡向正反应进行,此时v(正)>v(逆),
故答案为:否;大于.
点评 本题考查化学平衡的计算,为高频考点,侧重于学生的分析、计算能力的考查,本题涉及化学平衡常数及影响因素、化学平衡的计算等,难度中等,注意灵活运用三段式解题.


科目:高中化学 来源: 题型:选择题
| A. | $\frac{b}{a}$ | B. | $\frac{c}{a}$ | C. | $\frac{b-2c}{a}$ | D. | $\frac{b-c}{a}$ |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
| ① | ② | ③ | ④ | ⑤ |
| 物质所含的微粒数 | 固体体积 | 溶液的质量百分比浓度 | 标准状况下气体的摩尔体积 | 非标准状况下某物质的质量 |
| 阿伏加德罗常数 | 固体密度 | 溶液体积 | 标准状况下气体的体积 | 物质的摩尔质量 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 2NH3(g)△H=-92kJ/mol.
2NH3(g)△H=-92kJ/mol.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
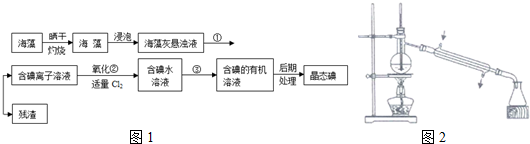
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①④②⑤③ | B. | ④①②⑤③ | C. | ②⑤④①③ | D. | ④⑤②①③ |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
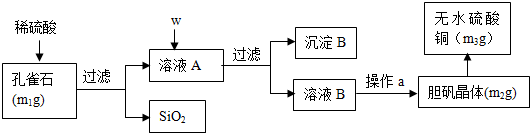
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com