
| 2x |
| 1-x+3-3x+2x |
| 1 |
| 3 |
| c2(NH3) |
| c(N2)c3(H2) |
| c2(NH3) |
| c(N2)c3(H2) |
| 2x |
| 1-x+3-3x+2x |
| 1 |
| 3 |
| ||
|
| 1 |
| 12 |
| ||
| 10min |
| ||
| 30mol |
| 1 |
| 12 |


 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
A�� ʵ��������ȡ��������ˮ |
B�� �����;ƾ� |
C�� �����������ƹ��� |
D��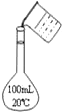 ����100mL 0.10 mol?L-1���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
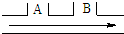 ij�����ų��ķ�ˮ�к��������ȣ�Ϊ��ȥ�÷�ˮ�е������ȣ�����ʹ��ˮ��Ϊ���ԣ����������ͼ�������ڷ�ˮ�ܵ�A��B���ֱ�ע��һ�������ռ���Һ������������Һ����������������ˮ������
ij�����ų��ķ�ˮ�к��������ȣ�Ϊ��ȥ�÷�ˮ�е������ȣ�����ʹ��ˮ��Ϊ���ԣ����������ͼ�������ڷ�ˮ�ܵ�A��B���ֱ�ע��һ�������ռ���Һ������������Һ����������������ˮ������ �鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A����״���£�2.24L��������������Ϊ0.1NA |
| B��0.3mol NO2��ˮ��ַ�Ӧת�Ƶĵ�����ĿΪ0.2NA |
| C��1mol Na2O2��������������������Ϊ4NA |
| D��60g SiO2��������Si-O������ĿΪ2NA��78g������C=C˫������ĿΪ3NA |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A����Na2CO3��Һ��ε��������У�CO32-+H+�THCO3- |
| B����ʳ�׳�ȥ��ˮƿ�е�ˮ����CO32-+2CH3COOH�T2CH3COO-+CO2��+H2O |
| C�����������Һ�м�������NaOH��Һ��H++OH-�TH2O |
| D����Al2��SO4��3��Һ�м��������ˮ��Al3++4NH3?H2O�TAlO2-+4NH4++2H2O |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��1 mol���������������������ĸ������ΪNA |
| B��14 g��ϩ�ͱ�ϩ�Ļ�����к��е�̼ԭ�ӵ���ĿΪNA |
| C��28 g C16O��28 g C18O�к��е���������Ϊ14 NA |
| D����״���£�22.4 L��������������������Һ��Ӧת�Ƶĵ�����Ϊ2 NA |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
A��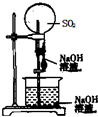 ��ѹװ�õĽ�ͷ�ι�ʹNaOH��Һȫ��������ƿ��Ƭ�̺��ֹˮ�� |
B��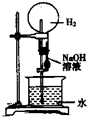 ��ѹװ�õĽ�ͷ�ι�ʹNaOH��Һȫ��������ƿ��Ƭ�̺��ֹˮ�� |
C�� �ù���װ�ô�װ�õ�a�����Ϲ����������ֹˮ�� |
D��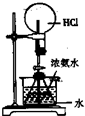 ��װ�õ�ˮ����������������Ũ���Ტ��ֹˮ�� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com