
����Ŀ����ϩ����Ҫ���л�����ԭ�ϣ�����������ϩΪԭ���Ʊ��ij����л����ʾ��ͼ��
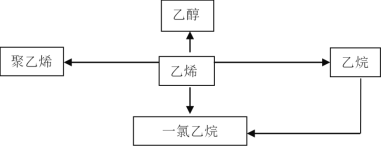
��1����ϩ�ĵ���ʽΪ________________����ͬϵ���ͨʽΪ_____________��
��2����ҵ������ϩ�Ʊ��Ҵ��Ļ�ѧ����ʽΪ____________________________��
��3������ϩ��Ĥ������ʳƷ��װ���ϣ�д������ϩ�ƾ���ϩ�Ļ�ѧ����ʽ��_______���˷�Ӧ����Ϊ_______��Ӧ��
��4���Ʊ�һ�����鳣�����ַ��������������������ڹ��������·�Ӧ��ȡ��������ϩ�ڼ���ʹ�ô��������������Ȼ������巴Ӧ��ȡ���Ƚ������Ʊ�����������Ϊ�ȽϺ�����һ�֣�___________��
���𰸡�![]() CnH2n CH2 = CH2 + H2O����CH3CH2OH nCH2 = CH2����
CnH2n CH2 = CH2 + H2O����CH3CH2OH nCH2 = CH2����![]() �Ӿ� ��
�Ӿ� ��
��������
������л���ת����ϵ��֪����ϩ������һ�������·����ӳɷ�Ӧ�������飻�����ڹ�������������������ȡ����Ӧ����һ�����飻��ϩ��ˮһ�������·����ӳɷ�Ӧ�����Ҵ�����ϩ���Ȼ��ⷢ���ӳɷ�Ӧ����һ�����飻��ϩһ�������·����Ӿ۷�Ӧ���ɾ���ϩ��
��1����ϩ�Ľṹ��ʽΪCH2 = CH2��������Ϊ̼̼˫��������ʽΪ![]() ����ϩ����ϩ����ϩ����ͨʽΪCnH2n���ʴ�Ϊ��
����ϩ����ϩ����ϩ����ͨʽΪCnH2n���ʴ�Ϊ��![]() ��CnH2n��
��CnH2n��
��2����ҵ������ϩ��ˮһ�������·����ӳɷ�Ӧ�Ʊ��Ҵ�����Ӧ�Ļ�ѧ����ʽΪCH2 = CH2 + H2O����CH3CH2OH���ʴ�Ϊ��CH2 = CH2 + H2O����CH3CH2OH��
��3����ϩһ�������·����Ӿ۷�Ӧ���ɾ���ϩ����Ӧ�Ļ�ѧ����ʽΪnCH2 = CH2����![]() ���ʴ�Ϊ��nCH2 = CH2����
���ʴ�Ϊ��nCH2 = CH2����![]() ��
��
��4�������������ڹ��������·���ȡ����Ӧ�����ɵ��������Ƕ����ȴ�����Ļ������ﲻΨһ���������������ȡһ�����飬��ϩ����±�����ܷ����ӳɷ�Ӧ�õ�±������һ������ϩ���Ȼ��ⷢ���ӳɼӳ���ȡһ�����飬����ֻ����һ�ִ����������飬�ʴ�Ϊ���ڡ�


 ����������������ϵ�д�
����������������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪һ���¶Ⱥ�ѹǿ��,�ϳɰ���Ӧ:N2(g)+3H2(g)=2NH3(g)����H=-92.0 kJ/mol,��1 mol N2��3 mol H2����һ�ܱ�������,���ֺ��º�ѹ,�ڴ�������ʱ���з�Ӧ,�ﵽƽ��ʱ,���N2��ת����Ϊ20%��������ͬ������,��ʼʱ��������г���2 mol NH3,��Ӧ�ﵽƽ��ʱ�������仯��(����)
A.����18.4 kJ����B.����73.6 kJ����
C.�ų�18.4 kJ����D.�ų�73.6 kJ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͬ�¡�ͬѹ�£�����������Ӧ�ų��������ֱ���a��b��c��ʾ����a��b��c�Ĺ�ϵ��(����)
2H2(g)��O2(g)===2H2O(g)����H����a kJ��mol��1 ����
2H2(g)��O2(g)===2H2O(l)����H����b kJ��mol��1�� ��
H2(g)��1/2O2(g)===H2O(g)����H����c kJ��mol��1�� ��
A.a��b�� b��2cB.a��b��cC.a��b��c��a/2D.���Ƚ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����б�ʾ��Ӧ��ѧ��Ӧ�����ӷ���ʽ��ȷ���ǣ� ��
A.MnO2��Ũ���ᷴӦ��Cl2��MnO2+4HCl![]() Mn2��+2Cl��+Cl2��+2H2O
Mn2��+2Cl��+Cl2��+2H2O
B.��������ˮ����Al(OH)3���壺Al3��+3H2O =Al(OH)3��+3H��
C.Na2O2����ˮ����O2��Na2O2+H2O =2Na��+2OH��+O2��
D.Ca(HCO3)2��Һ������NaOH��Һ��Ӧ��HCO3��+Ca2��+OH��= CaCO3��+H2O
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ʵ������ijЩ�������ȡ���ռ���β������װ����ͼ��ʾ��ʡ�Լг֡����Ⱥ;���װ�ã������ô�װ�úͱ����ṩ������������ʵ�飬�������ѡ����
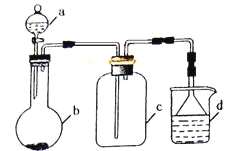
ѡ�� | a�е����� | b�е����� | c���ռ������� | d�е����� |
A | Ũ���� | Cu | NO2 | NaOH��Һ |
B | Ũ��ˮ | CaO | NH3 | H2O |
C | ϡ���� | Cu | NO | H2O |
D | Ũ���� | Cu | SO2 | ����NaHSO3��Һ |
A.AB.BC.CD.D
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������ȣ�ClO2�����Գ�ȥ��ҵ��ˮ�е��軯���Ӧ�����ӷ���ʽΪ��2ClO2+2CN-=2CO2��+N2��+2Cl-
���������գ�
��1��������Ӧ���漰Ԫ�ص�ԭ�Ӱ뾶�ɴ�С��˳����___������ԭ�Ӻ���������δ�ɶԵ��ӵ�Ԫ����___����Ƚ�̼�͵�Ԫ�طǽ�����ǿ��___����һ����ѧ��Ӧ����ʽ��ʾ����
��2���������Ȼ����Գ�ȥ��ˮ�е������ӣ�����ƽ���·�Ӧ��___��
ClO2+MnSO4+H2O��MnO2��+HCl+H2SO4
����Ӧ������0.2molMnO2�������ת��___����
��3���ȵ���һ��������Cl2Oÿ��ԭ�Ӷ��ﵽ8�����ȶ��ṹ�����ĵ���ʽΪ___��
��4����һ�ִ������軯����ˮ�ķ����ǵ�ⷨ�������ж�CN-����___���ϣ�ѡ���ţ�����������������Ӧ��CO2��N2���жϵ�������___��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������ӵ�������ֵΪNA�����������д������( )
�ٱ�״���£�2.24Lˮ�к���0.1 NA��ˮ����
�ڳ��³�ѹ�£�32gSO2 ���еķ�����ԼΪ3.01��1023
��2 molNaOH��Ħ������Ϊ80g/mol
��H2������Ħ�����ԼΪ22.4L/mol
�������£�32gO2��O3�Ļ�������к��е���ԭ����Ϊ2NA
��2mol/L��CaCl2��Һ��Cl-����ĿΪ4NA
�߳��³�ѹ�£�1mol�������е�ԭ����ΪNA
��11.2L�����к��� NA����ԭ��
���ڱ�״���£�22.4L��N2��N2O��ɵĻ�������У������еĵ�ԭ�ӵ����ʵ���Ϊ2mol
���״����14gCO���еĺ��������Ϊ10NA
A.�٢ۢܢޢ��B.�٢ܢݢޢ��
C.�٢ڢܢޢ��D.�ڢۢܢݢߢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������ۺ�������������ĩ��ϳ����ȼ�,ƽ���ֳ����ݡ���һ���ڸ����¶���ǡ����ȫ��Ӧ���������������������ַ�Ӧ;�ڶ���ֱ�Ӽ�������������������Һʹ֮��ַ�Ӧ��ǰ���������������������ʵ���֮��
A.1:1B.3:2C.2:3D.3:4
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ȡ��ϩʱ�������¶ȹ��߶���������Ӧ�������Ҵ���ŨH2SO4 ��Ӧ����SO2��CO2��ˮ������̿�ڡ�
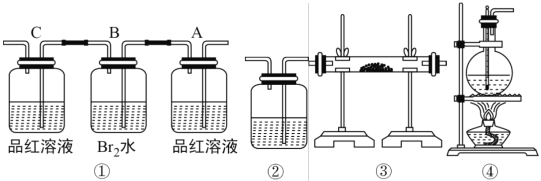
(1)�ñ��Ϊ�١��ܵ�ʵ��װ�����һ��ʵ�飬����֤������Ӧ��������к�CO2��SO2��ˮ������д��װ�õ�����˳���������������ҵ�������д��ţ���______��
(2)ʵ���װ�â��� A ƿ��������______������Ϊ__________�� B ƿ�е�������__________�� B ƿ��Һ����Ϊ__________���� C ƿ��Ʒ����Һ����ɫ���ɵõ�����Ϊ__________��
(3)װ�â��мӵĹ���ҩƷ��______����֤�����������______��װ�â���ʢ����Һ��_____����֤�����������______��
(4)����װ�â�������װ����λ�õ�����__________��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com