
【题目】有五种短周期元素,它们的结构、性质等信息如下表所示:
元素 | 结构、性质等信息 |
A | 是短周期元素(稀有气体元素除外)中原子半径最大的元素,含该元素的某种合金是原子反应堆的导热剂 |
B | 与A同周期,其最高价氧化物对应的水化物呈两性 |
C | 其气态氢化物极易溶于水,液态时常用作制冷剂 |
D | 是海水中除氢、氧元素外含量最多的元素,其单质或化合物也是自来水生产过程中常用的杀菌消毒剂 |
E | 元素原子的L电子层上有2对成对电子 |
请根据表中信息回答下列问题。
(1)A元素原子的核外电子排布式为___。
(2)B元素在元素周期表中的位置为___;离子半径:B___(填“>”或“<”)A。
(3)C元素原子的轨道表示式为___,其原子核外有___个未成对电子,能量最高的电子排布在轨道上,该轨道呈___形。
(4)D元素原子的核外电子排布式为___,D-的结构示意图为___。
(5)C、E元素的第一电离能的大小关系是___(用元素符号表示)。
(6)已知CD3分子中D元素显+1价,则该情况下,C、D元素的电负性大小关系是CD3___(用元素符号表示),CD3与水反应后的产物是___(填化学式)。
【答案】1s22s22p63s1(或[Ne]3s1) 第三周期第ⅢA族 < ![]() 3 哑铃 1s22s22p63s23p5(或[Ne]3s23p5)
3 哑铃 1s22s22p63s23p5(或[Ne]3s23p5) 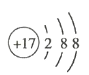 N>O N>Cl NH3(或NH3·H2O)和HClO
N>O N>Cl NH3(或NH3·H2O)和HClO
【解析】
短周期元素中,A是短周期中(除稀有气体外)原子半径最大的元素,该元素的某种合金是原子反应堆的导热剂,则A为Na;B与A同周期,其最高价氧化物的水化物呈两性,则B为Al;C元素的气态氢化物极易溶于水,可用作制冷剂,则C为N元素;D是海水中除氢、氧元素外含量最多的元素,其单质或化合物也是自来水生产过程中常用的消毒杀菌剂,则D为Cl,E是L层上有2对成对电子,则E为O,据此分析解答。
(1)A为Na,其核外电子排布式为1s22s22p63s1或[Ne]3s1;
(2)B为Al,其在元素周期表中的位置为第三周期第ⅢA族,Na+与Al3+的核外电子排布相同,核电荷数:Al3+>Na+,故离子半径:Al3+<Na+;
(3)C为N,其原子的轨道表示式为![]() ,其中有3个未成对电子,能量最高的电子排布在p轨道上,该轨道呈哑铃形;
,其中有3个未成对电子,能量最高的电子排布在p轨道上,该轨道呈哑铃形;
(4)D为Cl,其核外电子排布式为1s22s22p63s23p5或[Ne]3s23p5,Cl-的结构示意图为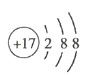 ;
;
(5)N、O分别位于第ⅤA族、第ⅥA族,因为N的2p轨道处于半充满状态,比较稳定,故第一电离能:N>O;
(6)NCl3分子中N显-3价,Cl显+1价,故N的电负性大于Cl,NCl3的水解产物为NH3(或NH3·H2O)和HClO。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】化学实验在学科中有着非常重要的作用,结合图示实验装置,下列相关分析的描述不正确的是( )
A.图1:盐桥中使用KCl溶液,电子的流向是Zn→G→Cu→CuSO4溶液→盐桥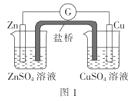
B.图2:可根据该实验验证铁的吸氧腐蚀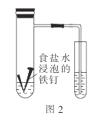
C.图3:在强酸和强碱的中和热实验中,强碱的浓度比强酸的略大
D.图4:根据两烧瓶中气体颜色的变化(热水中变深、冰水中变浅)可以判断反应2NO2(g)![]() N2O4(g)是一个放热反应
N2O4(g)是一个放热反应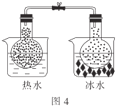
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一密闭容器中发生反应:3Fe(s)+4H2O(g)![]() Fe3O4(s)+4H2(g),下列判断正确的是( )
Fe3O4(s)+4H2(g),下列判断正确的是( )
A.升高反应温度对反应限度无影响
B.改变H2的浓度对正反应速率无影响
C.保持体积不变,充入N2反应速率增大
D.保持压强不变,充入N2反应速率减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】偏二甲肼与N2O4是常用的火箭推进剂,二者发生如下化学反应:(CH3)2NNH2(l)+2N2O4(l)====2CO2(g)+3N2(g)+4H2O(g)(Ⅰ)
(1)反应(Ⅰ)中氧化剂是_____________________________。
(2)火箭残骸中常出现红棕色气体,原因为:N2O4(g) ![]() 2NO2(g)(Ⅱ)当温度升高时,气体颜色变深,则反应(Ⅱ)为_______(填“吸热”或“放热”)反应。
2NO2(g)(Ⅱ)当温度升高时,气体颜色变深,则反应(Ⅱ)为_______(填“吸热”或“放热”)反应。
(3)一定温度下,反应(Ⅱ)的焓变为ΔH。现将1 mol N2O4充入一恒压密闭容器中,下列示意图正确且能说明反应达到平衡状态的是____________。

若在相同温度下,上述反应改在体积为1 L的恒容密闭容器中进行,平衡常数______(填“增大”“不变”或“减小”),反应3 s后NO2的物质的量为0.6 mol,则0~3 s内的平均反应速率v(N2O4)= ________mol·L-1·s-1。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现代工业生产中常用电解氯化亚铁的方法制得氯化铁溶液吸收有毒的硫化氢气体。工艺原理如下图所示。下列说法中不正确的是( )
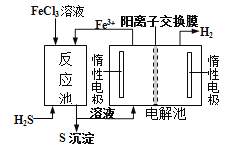
A. H+从电解池左槽迁移到右槽 B. 左槽中发生的反应是:2Cl--2e-=Cl2↑
C. 右槽的反应式: 2H++2e-=H2↑ D. FeCl3溶液可以循环利用
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Cu3N具有良好的电学和光学性能在电子工业领域、航空航天领域、国防领域、通讯领域以及光学工程等领域中,发挥着广泛的、不可替代的巨大作用。
(1)C、N、O三种元素的第一电离能由大到小的顺序为__。
(2)与N3-含有相同电子数的三原子微粒的空间构型是__。
(3)Cu+的电子排布式为__,其在酸性溶液中不稳定,可发生歧化反应生成Cu2+和Cu,但CuO在高温下会分解成Cu2O,试从结构角度解释高温下CuO为何会生成Cu2O:__。
(4)在Cu的催化作用下,乙醇可被空气氧化为乙醛,乙醛分子中碳原子的杂化方式是__,乙醛分子H-C-O的键角_(填“大于”“等于”或“小于”)乙醇分子中的H-C-O的键角。
(5)[Cu(H2O)4]2+为平面正方形结构,其中的两个H2O被Cl-取代有两种不同的结构,试画出Cu(H2O)2Cl2具有极性的分子的结构式:___。
(6)Cu3N的晶胞结构如图所示,N3-的配位数为__,Cu+的半径为apm,N3-的半径为bpm,Cu3N的密度为__g·cm-3(阿伏加德罗常数用NA表示)。
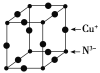
(7)肼(N2H4)又称联氨,是一种可燃性的液体,可用作火箭燃料。肼—空气燃料电池是一种碱性燃料电池,产物无污染,电解质溶液是20%~30%的KOH溶液。肼—空气燃料电池放电时,负极的电极反应式是__;
(8)发射神舟飞船的长征火箭用肼(N2H4,气态)为燃料,为了提高肼(N2H4)燃烧过程中释放的能量,常用NO2作氧化剂代替O2,这两者反应生成N2和水蒸气。
已知:①N2(g)+2O2(g)=2NO2(g) ΔH1=+67.7kJ·mol-1;②N2H4(g)+O2(g)=N2(g)+2H2O(g) ΔH2=-534kJ·mol-1,写出肼和NO2完全反应的热化学方程式:__。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组有机化合物中,不论两者以什么比例混合,只要总物质的量一定,则完全燃烧时生成的水的质量和消耗氧气的质量不变的是
A. CH4O,C3H4O5B. C3H6,C3H8O
C. C3H8,C4H6D. C2H6,C4H6O2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】类推的思维方法在化学学习与研究中常会产生错误的结论,因此类推的结论最终要经过实践的检验才能确定其正确与否。下表中有关推论正确的是( )
已知事实 | 推论 | |
A | 氯乙烷能发生消去反应 | 所有的卤代烃都能发生消去反应 |
B | 乙烯分子内所有原子在同一平面上 | 丙烯分子内所有原子在同一平面上 |
C | 乙烯在空气中燃烧有黑烟 | 苯在空气中燃烧产生的烟更浓 |
D | 烷烃的含碳量随碳原子数的增大而增大 | 炔烃的含碳量随碳原子数的增大而增大 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2020年2月15日,由国家科研攻关组的主要成员单位的专家组共同研判磷酸氯喹在细胞水平上能有效抑制新型冠状病毒(SARS-CoV-2)的感染。磷酸氯喹的结构如图所示,据此回答下列问题。
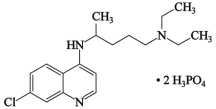
(1)C、N、O三种元素第一电离能从大到小的顺序为_____________;电负性χ(P)_____χ(Cl)(填“>”或“<”);
(2)磷酸氯喹中N原子的杂化方式为_____,NH3是一种极易溶于水的气体,其沸点比AsH3的沸点高,其原因是___________;
(3)磷化镓与砷化镓是两种由ⅢA族元素与ⅤA族元素人工合成的Ⅲ-Ⅴ族化合物半导体材料。其晶胞结构可看作金刚石晶胞内部的碳原子被P(As)原子代替,顶点和面心的碳原子被Ga原子代替。
①基态Ga原子核外电子排布式为__________;
②砷化镓晶体中含有的化学键类型为___________(填选项字母);
A.离子键 B.配位键 C.σ键 D.π键 E.极性键 F.非极性键
③磷化镓与砷化镓具有相似的晶体结构,其中熔点较高的是__________(填化学式),原因是_______________;
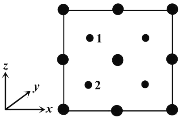
④以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置。称作原子分数坐标。如图为沿y轴投影的磷化镓晶胞中所有原子的分布图。若原子1的原子分数坐标为(0.25,0.25,0.75),则原子2的原子分数坐标为__________;若磷化镓的晶体密度为ρ g·cm-3,阿伏加德罗常数的值为NA,则晶胞中Ga和P原子的最近距离为__________ pm(用代数式表示)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com