
| ���� | ��� | �ڿ����м���ʱ������ | ����ˮ��Һ������� |
| X | ��ɫ��δ | ȼ��ʱ�ʳ��ɫ���������ų���ɫ����G | ������ |
| Y | ����ɫ���� | �����ۻ���Ȼ��ȼ�գ�����Ϊdz��ɫ���ų��д̼�����ζ������ | ������ |
| Z | ����ɫ���� | ȼ�գ�������ɫ���棬����dz��ɫ����F | ǿ���� |
 ��
�� ���� ��ɫ��ĩX��ȼ�գ������ɵ�������Һˮ����Һ�������ԣ���XΪ̼����������GΪCO2������ɫ����Y�ڿ����м������ۻ���ȼ�գ�����Ϊdz��ɫ���ų��д̼�����ζ�����壬YΪS���ʣ���������Ϊ������������ɫ����Zȼ�գ�������ɫ���棬ZӦΪNa������dz��ɫ����FΪNa2O2���Դ˽����⣮
��� �⣺��ɫ��ĩX��ȼ�գ������ɵ�������Һˮ����Һ�������ԣ���XΪ̼����������GΪCO2������ɫ����Y�ڿ����м������ۻ���ȼ�գ�����Ϊdz��ɫ���ų��д̼�����ζ�����壬YΪS���ʣ���������Ϊ������������ɫ����Zȼ�գ�������ɫ���棬ZӦΪNa������dz��ɫ����FΪNa2O2��
��1�������Ϸ�����֪XΪ̼��YΪ��ZΪ�ƣ�FΪ�������ƣ��ʴ�Ϊ��̼�����ƣ��������ƣ�
��2��GΪCO2������C=O����Ϊ���Լ�����̬ʱΪ���Ӿ��壬�ʴ�Ϊ���У����ӣ�
��3��Y��Z��Ӧ���ɵĻ�����ΪNa2S��Ϊ���ӻ��������ʽΪ ���ʴ�Ϊ�����ӣ�
���ʴ�Ϊ�����ӣ� ��
��
���� �����������ƶ�Ϊ���壬����Ԫ�ؼ��仯��������ʡ���ѧ����ȣ�Ϊ��Ƶ���㣬������ѧ���ķ��������Ŀ��飬�ۺ��Խϴ��Ѷ��еȣ�Ҫ���ճ���Ԫ�ؼ��䵥�ʺͻ���������ʣ�


 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | Cl- ��NO3-һ�����Բ�ͬ�Ĺ��� | B�� | SO42- ��NO3-��������ͬһ���� | ||
| C�� | Ag+ ��Na+ ��������ͬһ���� | D�� | Na+ ��NO3-һ������ͬһ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 �ֽ�һ������ͭƬ���뵽100mLϡ������������Ļ����Һ�У�ͭƬ��ȫ�ܽ⣨�������ε�ˮ�⼰��Һ����ı仯����
�ֽ�һ������ͭƬ���뵽100mLϡ������������Ļ����Һ�У�ͭƬ��ȫ�ܽ⣨�������ε�ˮ�⼰��Һ����ı仯�����鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �ں������ʵ�����FeBr2��FeI2����Һ�л���ͨ��Cl2��I-��Br-��Fe2+ | |
| B�� | �ں������ʵ�����Fe3+��Cu2+��H+����Һ�м���Zn��Fe3+��Cu2+��Fe2+��H+ | |
| C�� | �ں������ʵ�����Ba��OH��2��KOH����Һ��ͨ��CO2��Ba��OH��2��KOH��K2CO3��BaCO3 | |
| D�� | �������ʵ�����AlO2-��OH-��CO32-��Һ�У���μ������AlO2-��Al��OH��3��OH-��CO32- |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
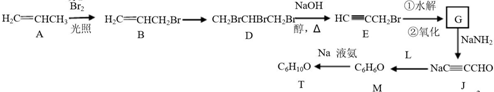
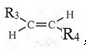 ����T�Ľṹ��ʽΪ
����T�Ľṹ��ʽΪ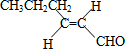 ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 1L 1mol•L-1NaHCO3��Һ�к���HCO3-��ĿΪNA | |
| B�� | 1mol Cl2������������Ӧ��ת�Ƶĵ�����Ϊ3NA | |
| C�� | ��״���£�22.4L�Ҵ��ķ�����ΪNA | |
| D�� | 17g H2O2�������ۼ�������Ϊ1.5NA |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com