
 周周清检测系列答案
周周清检测系列答案 轻巧夺冠周测月考直通高考系列答案
轻巧夺冠周测月考直通高考系列答案科目:高中化学 来源:2017届江苏省高三上第一次测试化学试卷(解析版) 题型:选择题
下列实验操作能够达到实验目的的是
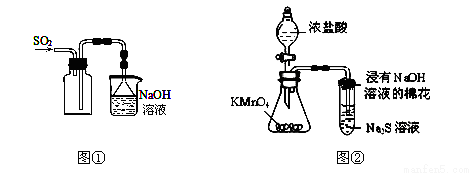
A. 实验室采用图①所示装置收集SO2
B. 可用图②所示装置比较KMnO4、Cl2、S的氧化性强弱
C. 除去NaHCO3溶液中的Na2CO3,可加入Ca(OH)2溶液后过滤
D. 称取0.40 g NaOH,置于100 mL容量瓶中,加水溶解,配制0.10 mol/L NaOH溶液
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
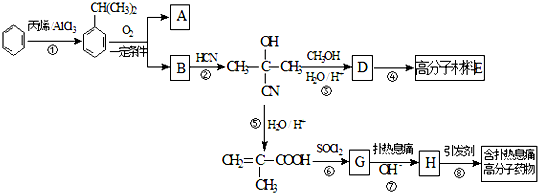
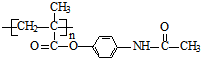 .
.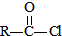
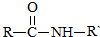 $\stackrel{Na溶液}{→}$RCOONa+R′-NH2
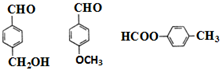
$\stackrel{Na溶液}{→}$RCOONa+R′-NH2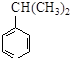 可转化为1mol A和1mol B,且A与FeCl3溶液作用显紫色,写出A的稀溶液与过量浓溴水发生反应的化学方程式
可转化为1mol A和1mol B,且A与FeCl3溶液作用显紫色,写出A的稀溶液与过量浓溴水发生反应的化学方程式 .
.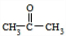 ;扑热息痛的结构简式为
;扑热息痛的结构简式为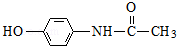 .
.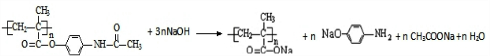 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 | |
| 2 | C | O | F | |||||
| 3 | Na | Mg | P | S | Cl |
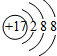 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
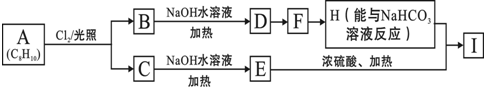
 +O2$→_{△}^{Cu}$2
+O2$→_{△}^{Cu}$2 +2H2O.
+2H2O.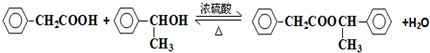 .
. .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Y的气态氢化物的沸点在同主族中最高,所以其气态氢化物最稳定 | |
| B. | Y、W形成的化合物与Y、Z形成的化合物中所含化学键相同 | |
| C. | 简单离子半径:Z>Y | |
| D. | 单质的氧化性:Y>W |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
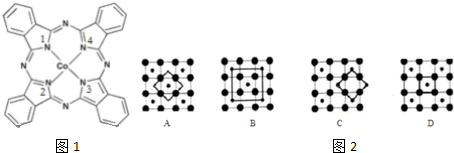
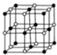 ),在该晶体中与一个钴原子等距离且最近的钴原子有12个;筑波材料科学国家实验室一个科研小组发现了在5K下呈现超导性的晶体,该晶体具有CoO2的层状结构(如图2所示,小球表示Co原子,大球表示O原子).下列用粗线画出的重复结构单元示意图不能描述 CoO2的化学组成的是D.
),在该晶体中与一个钴原子等距离且最近的钴原子有12个;筑波材料科学国家实验室一个科研小组发现了在5K下呈现超导性的晶体,该晶体具有CoO2的层状结构(如图2所示,小球表示Co原子,大球表示O原子).下列用粗线画出的重复结构单元示意图不能描述 CoO2的化学组成的是D.查看答案和解析>>
科目:高中化学 来源:2017届江苏省如皋市高三上学期质量调研一化学试卷(解析版) 题型:推断题
多巴胺是一种重要的中枢神经传导物质。用香兰素与硝基甲烷等为原料合成多巴胺的路线如下。
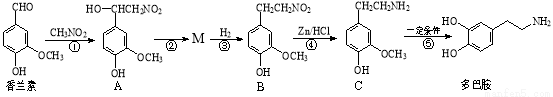
(1)下列说法正确的是 。
A.可用银镜反应鉴别香兰素和多巴胺
B.1 mol香兰素与溴水发生取代反应时,最多消耗3 mol Br2
C.有机物B分子中不含手性碳原子
D.多巴胺分子中最多有7个碳原子共平面
(2)有机物C中的含氧官能团的名称为 。
(3)反应①、②的反应类型分别为 。
(4)写出同时满足下列条件的A的一种同分异构体的结构简式 。
①具有α-氨基酸的共同结构片段;
②能与FeCl3溶液发生显色反应;
③由6种不同化学环境的氢原子。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com