
| A.晶体熔点达2500℃ | B.晶体不导电,溶于水导电 |
| C.晶体不导电,熔融能导电 | D.温度越高,溶解度越大 |
科目:高中化学 来源:不详 题型:填空题
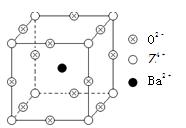
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 。
。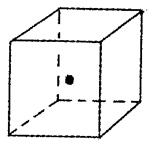
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 有A、C两元素的微粒是 。(写化学式)
有A、C两元素的微粒是 。(写化学式)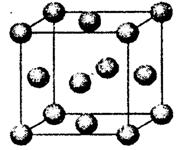
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题

查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| 选 项 | A | B | C | D |
| 晶体名称 | 硫酸钾 | 冰 | 二氧化硅 | 铝 |
| 晶体类型 | 离子晶体 | 分子晶体 | 原子晶体 | 金属晶体 |
| 组成晶体的粒子名称 | 阳、阴离子 | 分 子 | 原 子 | 铝离子、自由电子 |
| 熔化时需破坏的作用力 | 离 子 键 | 共价键、氢键、范德华力 | 共价键 | 金属键 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 性键
性键| A.只有②⑤⑥⑦ | B.只有②⑤⑥ | C.只有①②③⑤⑥⑧ | D.只有②③⑤⑥⑦ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
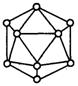
| A.20个,60个,360° | B.12个,30个,60° |
| C.9个,18个,45° | D.18个,54个,90° |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com