
分析 (1)用氧化物表示物质的组成时,要按照:活泼金属氧化物•不活泼金属氧化物•SiO2•H2O的顺序来书写;
(2)镁能在二氧化碳中燃烧;
(3)在NaHSO4溶液中滴加Ba(OH2)溶液至溶液呈中性,反应生成硫酸钡、硫酸钠和水;
(4)①煅烧黄铁矿生成氧化铁和二氧化硫;
②亚铁离子的还原性大于溴离子,氯气不足时亚铁离子优先反应.
解答 解:(1)用氧化物表示物质的组成时,要按照:活泼金属氧化物•不活泼金属氧化物•SiO2•H2O的顺序,故NaAl(SiO3)2的组成可以表示为:Na2O•Al2O3•4SiO2,
故答案为:Na2O•Al2O3•4SiO2;
(2)镁能在二氧化碳中燃烧,化学方程式为:2Mg+CO2$\frac{\underline{\;点燃\;}}{\;}$2MgO+C,
故答案为:2Mg+CO2$\frac{\underline{\;点燃\;}}{\;}$2MgO+C;
(3)在NaHSO4溶液中滴加Ba(OH2)溶液至溶液呈中性,反应生成硫酸钡、硫酸钠和水,离子方程式:Ba2++2OH-+2H++SO42-═2H2O+BaSO4↓;
故答案为:Ba2++2OH-+2H++SO42-═2H2O+BaSO4↓;
(4)①煅烧黄铁矿生成氧化铁和二氧化硫,化学方程式为:4FeS2+11O2$\frac{\underline{\;高温\;}}{\;}$2Fe2O3+8SO2,
故答案为:4FeS2+11O2$\frac{\underline{\;高温\;}}{\;}$2Fe2O3+8SO2;
②向FeBr2中通入等量Cl2,亚铁离子优先反应,然后部分溴离子被氯气氧化,反应的离子方程式为:2Fe2++2Br-+2Cl2═2Fe3++Br2+2Cl-,
故答案为:2Fe2++2Br-+2Cl2═2Fe3++Br2+2Cl-.
点评 本题考查了化学方程式的书写、离子方程式书写,题目难度不大,明确发生反应的实质为解答关键,注意熟练掌握离子方程式的书写原则,试题培养了学生的分析能力及灵活应用能力.


 王后雄学案教材完全解读系列答案
王后雄学案教材完全解读系列答案 海淀课时新作业金榜卷系列答案
海淀课时新作业金榜卷系列答案 期末金牌卷系列答案
期末金牌卷系列答案 轻松课堂标准练系列答案
轻松课堂标准练系列答案科目:高中化学 来源: 题型:选择题
| A. | 1:2 | B. | 1:4 | C. | 2:1 | D. | 4:1 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
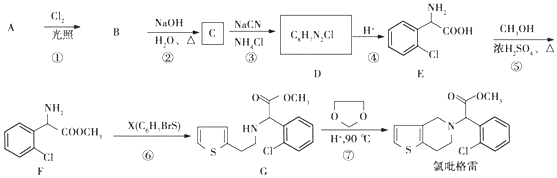
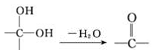 ;②
;②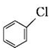 中氯原子较难水解;③RCHO$→_{NH_{4}Cl}^{NaCN}$
中氯原子较难水解;③RCHO$→_{NH_{4}Cl}^{NaCN}$
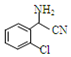 ;C分子中最多有14个原子共平面.
;C分子中最多有14个原子共平面.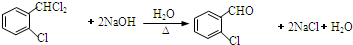 .
.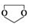 ,需要经历的反应类型有②①③④③(填写编号).①加成反应 ②消去反应 ③取代反应 ④氧化反应 ⑤还原反应,写出制备化合物
,需要经历的反应类型有②①③④③(填写编号).①加成反应 ②消去反应 ③取代反应 ④氧化反应 ⑤还原反应,写出制备化合物 的最后一步反应HOCH2CH2OH+HCHO$\stackrel{酸}{→}$
的最后一步反应HOCH2CH2OH+HCHO$\stackrel{酸}{→}$ .
.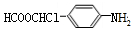 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 制备氯气时严格检查装置的气密性,并设置尾气吸收装置 | |
| B. | 稀释浓硫酸时,将水倒入浓硫酸中,使用玻璃棒不断搅拌 | |
| C. | 在敞口容器中进行铜与浓硝酸的反应,并观察生成的气体 | |
| D. | 向一支试管中加入少量水,向其中投入一块黄豆大小的钠 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com