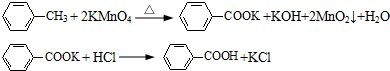
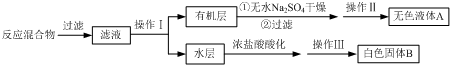
海带成分中碘的检验实验方案设计
①取10g食用干海带,用刷子把干海带表面附着物刷净,不要用水洗.将海带剪碎,用酒精润湿放入瓷坩埚中,把坩埚置于泥三角上.用酒精灯灼烧盛有海带的坩埚,至海带完全烧成炭黑色灰后,停止加热,自然冷却.将坩埚内海带灰放至小烧杯中,再加入15mL蒸馏水,不断搅拌,煮沸4min~5min,使可溶物溶解,10分钟后过滤.将滤液分成四份放入试管中,并标为1、2、3、4号.
②在1号试管中滴入6滴稀硫酸后,再加入约3mL H
2O
2溶液,观察现象.滴入1%淀粉液1~2滴,观察现象.
③在2号试管中加入2mL新制的饱和氯水,振荡溶液,观察现象.2分钟后把加入氯水的溶液分成两份.其中甲中再滴入1%淀粉液1~2滴,观察现象.乙溶液中加入2mL CCl
4,振荡萃取,静置2分钟后观察现象.
④在3号试管中加入食用碘盐3g,振荡使之充分溶解后滴入6滴稀硫酸.在滴入1%淀粉液1~2滴,观察现象.
⑤在4号试管中加入硝酸银溶液,振荡,再加入稀硝酸溶液. 原想利用反应Ag
++I
-=AgI↓生成黄色沉淀来检验碘离子.通过实验发现生成白色沉淀.用此方法检验碘元素失败.
完成下面的实验现象及分析
实验现象及分析
| 试管号 | 加入试剂 | 实验现象 | 离子方程式 |
| 1号 | 稀硫酸、H2O2、淀粉液 | 溶液立刻由褐色变成蓝色 | (1) |
| 2号 甲 | 新制的饱和氯水、1%淀粉液 | (2) | 2I-+Cl2=I2+2Cl- |
| 2号 乙 | 新制的饱和氯水、CCl4 | (3) | |
| 3号 | 食用碘盐、稀硫酸、1%淀粉液 | 溶液立刻由无色变成蓝色 | (4) |
(5)导致第⑤步失败的可能原因是
.
(6)将AgCl白色沉淀加入到KI溶液中搅拌,看到的现象是沉淀由白色转化为黄色,说明K
sp(AgCl)>K
sp(AgI),“说明”正确吗?
(填“正确”或“不正确”),理由是
.




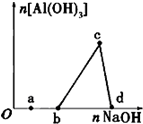 一定量的酸性AlCl3 溶液中逐滴加入NaOH溶液,生成沉淀Al(OH)3的量随NaOH加入量的变化关系如图所示.则下列离子组在对应的溶液中一定能大量共存的是( )
一定量的酸性AlCl3 溶液中逐滴加入NaOH溶液,生成沉淀Al(OH)3的量随NaOH加入量的变化关系如图所示.则下列离子组在对应的溶液中一定能大量共存的是( )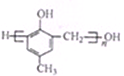 )的合成路线如下:
)的合成路线如下: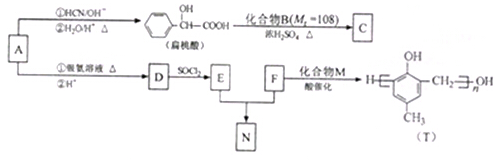
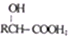

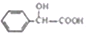 )有多种同分异构体,属于甲酸酯且含酚羟基的同分异构体共有
)有多种同分异构体,属于甲酸酯且含酚羟基的同分异构体共有