
 .
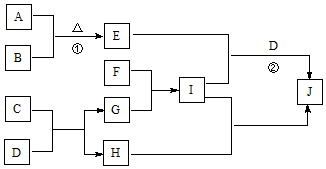
.分析 由D是最常见的无色液体,可推出D为H2O,E、F、H都是常见的气体,且E、F都可用于漂白即Cl2和SO2,H是空气中主要成分之一,可推出H为O2,又A是常见的金属氧化物,B是常见的强酸,并且A和B加热生成E即MnO2和浓HCl反应生成Cl2,所以推出A为MnO2,B为浓HCl,E为Cl2,F为SO2,C是常见的金属氧化物
与D(H2O)反应生成H即O2,所以C为Na2O2,G为NaOH,F和G生成I,则I为Na2SO3,I和H生成J,E、D和I生成J,则J为Na2SO4,据此解答该题.
解答 解:(1)根据以上分析,D的化学式为H2O,故答案为:H2O;
(2)根据以上分析,G为NaOH,电子式为 ,故答案为:
,故答案为: ;
;
(3)反应①为MnO2和浓HCl在加热条件发生反应生成Cl2,反应方程式为:MnO2+4HCl(浓)$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O,故答案为:MnO2+4HCl(浓)$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O;
(4)反应②为Cl2,Na2SO3和水反应生成Na2SO4,则离子方程式为Cl2+SO32-+H2O=SO42-+2Cl-+2H+,故答案为:Cl2+SO32-+H2O=SO42-+2Cl-+2H+.
点评 本题考查无机物的推断,题目难度较大,解答本题的关键是正确推断物质的种类,推断时,要根据物质的特殊性质作为突破口,学习中注重相关知识的积累.


科目:高中化学 来源: 题型:选择题
| A. | 实验→分类(预测Br2的化学性质)→观察(得出Br2的物理性质)→比较并得出结论 | |
| B. | 分类(预测Br2的化学性质)→观察(得出Br2的物理性质)→实验→比较并得出结论 | |
| C. | 观察(得出Br2的物理性质)→实验→分类(预测Br2的化学性质)→比较并得出结论 | |
| D. | 观察(得出Br2的物理性质)→分类(预测Br2的化学性质)→实验→比较并得出结论 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | AlCl3 | B. | NaHCO3 | C. | Na2CO3 | D. | Al2(SO4)3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 锌与CH3COOH溶液反应:Zn+2H+═Zn2++H2↑ | |
| B. | 氢氧化铝与稀硝酸反应:H++OH-═H2O | |
| C. | CuCl2溶液与铁粉反应:3Cu2++2Fe═3Cu+2Fe3+ | |
| D. | MgCl2溶液与氨水反应:Mg2++2NH3•H2O═Mg(OH)2↓+2NH4+ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
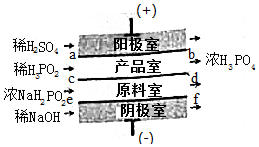 次磷酸(H3PO2)位一元酸,具有较强的还原性.可利用NaH2PO2为原料,通过四室电渗析法制备,工作原理如图所示,采用惰性电极,ab,cd,ef均为只允许阳离子(或阴离子)通过的离子交换膜,分别称为阳膜(或阴离子),下列说法描述错误的是( )
次磷酸(H3PO2)位一元酸,具有较强的还原性.可利用NaH2PO2为原料,通过四室电渗析法制备,工作原理如图所示,采用惰性电极,ab,cd,ef均为只允许阳离子(或阴离子)通过的离子交换膜,分别称为阳膜(或阴离子),下列说法描述错误的是( )| A. | 阳极室反应为:2H2O-4e-=O2↑+4H+ | |
| B. | ab,ef均为阳膜,cd为阴膜 | |
| C. | 若将稀H2SO4改为H3PO3,撤去ab膜,产品中总混有杂质的原因是:H3PO2在阳极放电而被氧化生成H3PO4 | |
| D. | 通电后产品室中的H+离子向原料室迁移 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
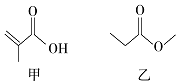
| A. | 甲、乙互为同分异构体 | |
| B. | 甲、乙都能发生取代、加成反应 | |
| C. | 与甲具有相同官能团的同分异构体还有2种 | |
| D. | 与乙具有相同官能团的同分异构体还有2种 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氯化铁溶液中加入足量的氨水:Fe3++3OH-═Fe(OH)3↓ | |
| B. | 铁片与稀硝酸反应Fe+2H+═Fe2++H2↑ | |
| C. | 氯气通入氯化亚铁溶液:Cl2+Fe2+═2Cl-+Fe3+ | |
| D. | 氢氧化铝溶于氢氧化钠溶液:Al(OH)3+OH-═AlO2-+2H2O |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com