
| A. | 在pH=1的溶液中:NH4+、ClO-、Cl- | |
| B. | 有SiO32-存在的溶液中:Na+、SO42-、Cl- | |
| C. | 有NO3-存在的溶液中:H+、Ba2+、Fe2+ | |
| D. | 室温下,水电离的c水(H+)=1.0×10-13mol•L-1溶液中:Na+、S2-、AlO2- |
分析 A.在pH=1的溶液显酸性,离子之间发生氧化还原反应;
B.该组离子之间不反应;
C.离子之间发生氧化还原反应;
D.室温下,水电离的c水(H+)=1.0×10-13mol•L-1溶液,为酸或碱溶液.
解答 解:A.在pH=1的溶液显酸性,H+、ClO-、Cl-发生氧化还原反应,不能大量共存,故A错误;
B.该组离子之间不反应,可大量共存,故B正确;
C.H+、NO3-、Fe2+发生氧化还原反应,不能大量共存,故C错误;
D.室温下,水电离的c水(H+)=1.0×10-13mol•L-1溶液,为酸或碱溶液,酸溶液中不能大量存在S2-、AlO2-,故D错误;
故选B.
点评 本题考查离子的共存,为高频考点,把握习题中的信息及常见离子之间的反应等为解答的关键,侧重分析与应用能力的考查,注意复分解反应、氧化还原反应的判断,题目难度不大.


 千里马走向假期期末仿真试卷寒假系列答案
千里马走向假期期末仿真试卷寒假系列答案科目:高中化学 来源:2016-2017学年宁夏卫一高一上10月月考化学b卷(解析版) 题型:选择题
下列仪器常用于物质分离的是
①漏斗 ②试管 ③蒸馏烧瓶 ④天平 ⑤分液漏斗 ⑥研钵
A.①③⑤ B.①②⑥ C.①③④ D.①③⑥
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
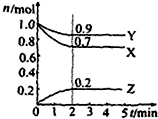 某温度时在2L容器中X、Y、Z三种物质的物质的量(n)随时间(t)变化的曲线如图所示,由图中数据分析:
某温度时在2L容器中X、Y、Z三种物质的物质的量(n)随时间(t)变化的曲线如图所示,由图中数据分析:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | HF的热稳定性很好,是因为HF分子间存在氢键 | |
| B. | 构成单质的分子内不一定存在共价键 | |
| C. | 由非金属元素组成的化合物不一定是共价化合物 | |
| D. | NaCl晶体熔化,需要破坏离子键 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
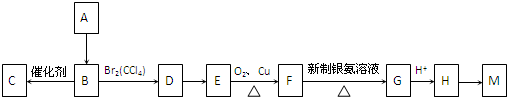
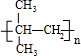 ,M的结构简式为
,M的结构简式为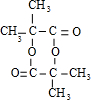 .
.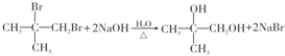 ;
;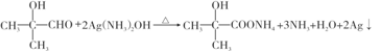 .
.查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 在蒸馏水中滴加浓硫酸,KW不变 | |
| B. | 在硫化钠稀溶液中,c(H+)═c(OH-)-2c(H2S)-c(HS-) | |
| C. | 氯化钠溶液和醋酸铵溶液均显中性,但两溶液中水的电离程度不相同 | |
| D. | pH=1的强酸溶液加水稀释后,溶液中各离子浓度均减小 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①③④⑤ | B. | ②③⑤⑦ | C. | ①④⑥⑦ | D. | 全部 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
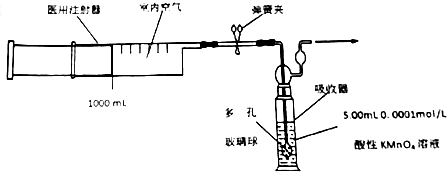
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com