
下列叙述正确的是
A.强电解质都是离子化合物,因此NaCl是离子化合物
B.醋酸溶液的导电能力可能比稀硫酸强
C.SO3溶于水,其水溶液能导电,SO3是电解质
D.硫磺是单质,不导电,因此硫磺是非电解质
 新课标阶梯阅读训练系列答案
新课标阶梯阅读训练系列答案 口算心算速算应用题系列答案
口算心算速算应用题系列答案科目:高中化学 来源: 题型:
关于下列各装置图的叙述中,不正确的是:
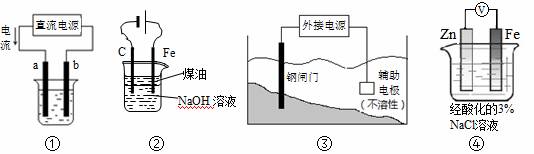
A.用装置①精炼铜,则a极为粗铜,电解质溶液为CuSO4溶液
B.用图②装置实验室制备白色Fe(OH)2
C.装置③中钢闸门应与外接电源的正极相连
D.装置④中电子由Zn流向Fe,Zn极发生氧化反应
查看答案和解析>>
科目:高中化学 来源: 题型:
将3.84 g Fe和Fe2O3的混合物溶于120 mL的盐酸,刚好完全反应,生成0.03 mol H2,若反应后的溶液中无Fe3+,且溶液体积不变,试求:
(1)原混合物中Fe2O3的质量为 ;
(2)原盐酸的物质的量浓度为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
NA表示阿伏加德罗常数,下列说法正确的是( )
A.1 mol Na与足量O2反应生成Na2O或Na2O2均失去NA个电子
B.1 mol Al分别放入足量的冷的浓HNO3、稀HNO3中,反应后转移的电子均为3NA
C.各5.6 g铁分别与足量的盐酸、氯气反应,电子转移总数均为0.3NA
D.24 g镁与足量的盐酸或NaOH溶液反应转移的电子数目均为2NA
查看答案和解析>>
科目:高中化学 来源: 题型:
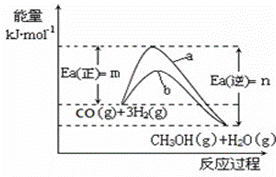 |  | ||
(1)写出合成甲醇反应的热化学方程式 ;
图1 图2
(2)在图中曲线 (填“a”或“b”)表示加入催化剂的能量变化曲线。
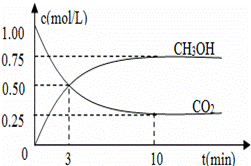
(3)在体积为l L的密闭容器中,充入lmolCO2和3molH2,测得CO2和CH3OH(g)的浓度随时间变化如图2所示.
①从反应开始到平衡,氢气的平均反应速率v(H2)=___________mol/(L·min)。
②该反应的平衡常数为__________________,升高温度,K值 (填“增大”、“减小”或“不变”)。
③下列措施中能使n(CH3OH)/n(CO2)增大的是___________。
A.升高温度 B.充入He(g),使体系压强增大
C.将H2O(g)从体系中分离 D.再充入1mol CO2和3mol H2
(4)在载人航天器的生态系统中,不仅要求分离去除CO2,还要求提供充足的O2。某种电化学装置可实现如下转化:2CO2=2CO+O2,CO可用作燃料。已知该反应的阳极反应为:4OH――4e―=O2↑+2H2O,则阴极反应式为:_______________________________ 。
有人提出,可以设计反应2CO=2C+O2(△H>0、△S<0)来消除CO的污染。请你判断是否可行并说出理由:__________________________ 。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列氧化还原反应中,水作为氧化剂的是
A.CO+H2O(g)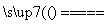 CO2+H2 B.3NO2+H2O===2HNO3+NO
CO2+H2 B.3NO2+H2O===2HNO3+NO
C.2Na2O2+2H2O===4NaOH+O2↑ D.2F2+2H2O===4HF+O2
查看答案和解析>>
科目:高中化学 来源: 题型:
锌与很稀的硝酸反应生成硝酸锌、硝酸铵和水。当生成1 mol硝酸锌时,被还原的硝酸的物质的量为A.2 mol B.1 mol C.0.5 mol D.0.25 mol
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于物质的分类说法正确的是:
A.金刚石、白磷都属于单质 B.漂白粉、石英都属于纯净物
C.氯化铵、次氯酸都属于强电解质 D.葡萄糖、蛋白质都属于高分子化合物
查看答案和解析>>
科目:高中化学 来源: 题型:
已知常温下,在溶液中发生如下反应:① 16H++10Z-+2XO4-=2X2++5Z2+8H2O;
②2A2++B2=2A3++2B-; ③2B-+Z2=B2+2Z-由此推断下列说法错误的是
A. 反应2A3++2Z-= Z2+2A2+可以进行
B. Z元素在①反应中被氧化,在③反应中被还原
C. 还原性由强到弱的顺序是A2+,B-,Z-,X2+
D. 氧化性由强到弱的顺序是XO4-,Z2,B2,A3+
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com