
| 1 |
| 2 |


科目:高中化学 来源: 题型:阅读理解
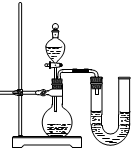 (2009?韶关一模)某兴趣小组同学为证明NaOH溶液与稀盐酸发生了中和反应,从不同角度设计了如下实验方案,并进行实验.
(2009?韶关一模)某兴趣小组同学为证明NaOH溶液与稀盐酸发生了中和反应,从不同角度设计了如下实验方案,并进行实验. HCO3-+OH-
HCO3-+OH- HCO3-+OH-
HCO3-+OH-| 编号 | 盐酸 | NaOH溶液 | △t/℃ |
| 1 | 3.65% | 2.00% | 3.5 |
| 2 | 3.65% | 4.00% | x |
| 3 | 7.30% | 8.00% | 14 |
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
查看答案和解析>>
科目:高中化学 来源:2011-2012学年浙江省高三10月份月考化学试卷 题型:实验题
(12分) 由几种盐溶于水中形成的一瓶澄清的溶液,其中可能含有NH4+、Na+、Mg2+、Ba2+、Al3+、Fe3+、Cu2+、Cl-、Br-、I-、NO3-、CO32-、SO32-、SO42-中的几种。取该溶液进行以下实验:
(1)用pH试纸检验,pH试纸呈红色。排除 离子的存在。
(2)取出部分溶液,加入少量CCl4及几滴新制氯水,经振荡CCl4层呈紫红色。排除
离子存在。
(3)另取部分溶液,逐渐向其中加入NaOH溶液,使溶液从酸性逐渐变为碱性,在滴加过程中和滴加完毕后,均无沉淀产生。则可排除 离子的存在。
(4)另取部分上述碱性溶液,向其中加入Na2CO3溶液,有白色沉淀生成。证明
离子存在,又排除 离子存在。
(5)根据上述实验事实能否确定NH4+是否存在,若能,请简述理由 ,若不能,请简述检验它的方法 。
(6)原溶液一定存在的离子有 ,不能确定的离子有 。
查看答案和解析>>
科目:高中化学 来源:2009年福建省福州市福清市高考化学模拟试卷(解析版) 题型:填空题
| 编号 | 盐酸 | NaOH溶液 | △t/℃ |
| 1 | 3.65% | 2.00% | 3.5 |
| 2 | 3.65% | 4.00% | x |
| 3 | 7.30% | 8.00% | 14 |

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com