
若以NA代表阿伏加德罗常数的值,下列说法中正确的是( )
A.1 mol Na 跟足量H2O反应得到电子的数目为NA
B.常温常压下,16 g甲烷(CH4)所含电子数为NA
C.标准状况下,22.4 L 酒精所含的分子数目为NA
D.常温常压下,6 g O2和26 g O3混合气体中的原子总数为2NA
科目:高中化学 来源:2016-2017学年广东省高一上大考二化学卷(解析版) 题型:选择题
下列各组离子中能大量共存的是
A.无色溶液中:K+、Na+、MnO4﹣、SO42﹣
B.在酸性溶液中:Mg2+、Na+、SO42﹣、Cl﹣
C.能使pH试纸变蓝色的溶液:Cl﹣、HCO3﹣、SO42﹣、NH4+
D.碱性溶液中:K+、Cl﹣、NO3﹣、Cu2+
查看答案和解析>>
科目:高中化学 来源:2016-2017学年黑龙江省高一12月月考化学试卷(解析版) 题型:选择题
下列叙述中不正确的是
A.Na2O2是淡黄色固体, Na2O 是白色固体, 二者都能与水反应生成 NaOH
B.钠质地柔软,可用小刀切割,保存在煤油中
C.钠的还原性很强,只能以化合态存在于自然界
D.Na2O与CO2发生化合反应生成Na2CO3,Na2O2与CO2发生置换反应生成 O2
查看答案和解析>>
科目:高中化学 来源:2017届宁夏高三上月考四化学试卷(解析版) 题型:选择题
设NA表示阿伏加德罗常数的值,下列说法正确的是( )
A.0.1 mol·L-1的NaHCO3溶液中,含有HCO3-与CO32-的数目之和为0.1 NA
B.0.1mol•L-1 Na2SO3溶液中:c(Na+)+c(H+)=2c(SO3 2-)+c(HSO 3-)+c(OH-)
C.等浓度的系列稀溶液:①硫酸氢钠、②乙酸钠、③醋酸、④碳酸氢钠、⑤硝酸钾、⑥苯酚钠、⑦氢氧化钠、⑧硫酸,它们的PH由小到大排列的为①③⑤②⑥④⑦⑧
D.25℃,由水电离出的C(H+)=1×10-12 mol·L-1 的溶液中以下离子Na+、NH4+、I-、NO3-一定能大量共存
查看答案和解析>>
科目:高中化学 来源:2017届宁夏高三上月考四化学卷(解析版) 题型:选择题
X、Y、Z、W、R属于短周期主族元素。X的原子半径是短周期主族元素中最大的,Y元素的单质常通过分离液态空气得到,Z元素的单质是常见的半导体材料,W与Z同族,R与Y同族,其单质有杀菌作用。下列叙述不正确的是( )
A. X与Y形成的两种化合物中阴、阳离子的个数比均为1∶2,且均能与水反应。
B. 根据非金属性强弱,不可能由Z的最高价氧化物制出W的最高价氧化物。
C. Y的简单氢化物的沸点和热稳定性均大于R的简单氢化物。
D. 向两份BaCl2溶液中分别通入RY2、WY2,均无白色沉淀生成,但一段时间后,通入RY2的一份中可能产生沉淀。
查看答案和解析>>
科目:高中化学 来源:2017届江苏省高三12月月考化学试卷(解析版) 题型:实验题
某研究小组同学通过下列流程制取不溶于水和稀硫酸的黄钾铵铁矾[KNH4Fex(SO4)y(OH)z],并通过实验测定样品中黄钾铵铁矾的有关组成。
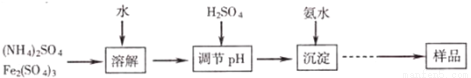
实验测定:
①称取一定质量的样品加入稀盐酸中充分溶解,将所得溶液转移至容量瓶并配制成l00mL溶液A;
②量取25.00mL溶液A,加入盐酸酸化的BaCl2溶液至沉淀完全,过滤、洗涤、干燥至恒重,得到白色固体9.32g;
③量取25.00mL溶液A,加入足量KI,用2.000mol·L﹣1Na2S2O3溶液进行滴定(已知反应为I2+2Na2S2O3═2NaI+Na2S4O6,消耗30.00mL Na2S2O3溶液至终点。
(1)在[KNH4Fex(SO4)y(OH)z]中x、y、z的代数关系式为 。
(2)若加入H2SO4将pH调节为2,则溶液c(Fe3+)应为 mol·L﹣1。(已知Ksp[Fe(OH)3]=4.0×10﹣38)
(3)实验测定②中检验沉淀是否完全的方法是 。
(4)根据以上实验数据计算样品中的n(Fe3+)∶n(SO42﹣)。(写出计算过程)
查看答案和解析>>
科目:高中化学 来源:2017届江苏省高三12月月考化学试卷(解析版) 题型:选择题
下列有关说法正确的是
A .常温下,pH=3的盐酸、醋酸分别用水稀释m倍、n倍后pH相同,则m<n
.常温下,pH=3的盐酸、醋酸分别用水稀释m倍、n倍后pH相同,则m<n
B.ΔH<0,△S>0的反应在一定条件下一定可以自发进行
C.以Al作阳极,Fe作阴极,可以实现铁上镀铝
D.工业合成SO3不采用高压是因为增大压强对SO2的转化率影响不大
查看答案和解析>>
科目:高中化学 来源:2016-2017学年浙江省高一上期中化学试卷(解析版) 题型:填空题
氧化还原反应中实际上包含氧 化和还原两个过程。下面是一个还原过程的反应式:NO3-+4H++3e-=NO↑+2H2O,已知KMnO4、Na2CO3、FeO、Fe2(SO4)3四种物质中的一种物质能使上述还原过程发生。
化和还原两个过程。下面是一个还原过程的反应式:NO3-+4H++3e-=NO↑+2H2O,已知KMnO4、Na2CO3、FeO、Fe2(SO4)3四种物质中的一种物质能使上述还原过程发生。
(1)写出并配平该氧化还原反应的方程式: 。
(2)反应中硝酸体现了 性质。
(3)反应中若产生0.2mol气体,则转移电子的物质的量是 mol。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年河南省高一上月考二化学卷(解析版) 题型:选择题
同温同压下, a g 甲气体和 2a g 乙气体所占的体积之比为 1: 2,根据阿伏加德罗定律判断,下列叙述不正确的是( )
A. 同温同压下甲和乙的密度之比为 1: 1
B. 甲与乙的相对分子质量之比为 1: 1
C. 同温同体积下等质量的甲和乙的压强之比为 1: 1
D. 等质量的甲和乙中的原子数之比为 1: 1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com