
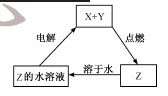
纯净物X、Y、Z转化关系如右图所示,下列判断正确的是
 A. X可能是金属铜
A. X可能是金属铜
B. Y不可能是氢气
C. Z可能是氯化钠
D. Z可能是二氧化硫
科目:高中化学 来源: 题型:
2013年初,某媒体报道了“皮革奶”事件,不法厂商将皮革下脚料水解后掺入奶粉以提高奶粉中蛋白质的含量。下列说法不正确的是( )。
A.动物皮革的主要成分是蛋白质
B.蛋白质水解的最终产物是氨基酸
C.皮革鞣制过程中使用的K2Cr2O7会使蛋白质盐析
D.利用盐析后可以再溶解的性质可分离提纯蛋白质
查看答案和解析>>
科目:高中化学 来源: 题型:
下列措施不合理的是
A.用SO2漂白纸浆和草帽辫
B.用硫酸清洗锅炉中的水垢
C.高温下用焦炭还原SiO2制取粗硅
D.用Na2S做沉淀剂,除去废水中的Cu2+和Hg2+
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于硫酸工业生产过程的叙述错误的是
A.在接触室中使用铁粉作催化剂
B.在接触室中运用热交换技术可充分利用能源
C.把硫铁矿磨成细粉末,可以提高原料的利用率
D.该反应采用450-500℃主要是因为该温度下催化剂活性好
查看答案和解析>>
科目:高中化学 来源: 题型:
在通风橱中进行下列实验:
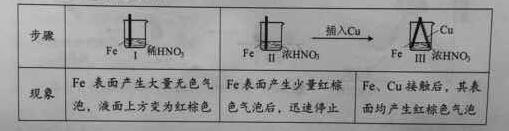
下列说法中不正确的是:
A、 Ⅰ 种气体有无色变红棕色的化学方程式为:2NO+O2=2NO2
B、 Ⅱ中的现象说明Fe表面形成致密的氧化层,阻止Fe进一步反应
C、 对比Ⅰ 、Ⅱ中现象,说明稀HNO3的氧化性强于浓HNO3
D、 针对Ⅲ中现象,在Fe、Cu之间连接电流计,可判断Fe是否被氧化
查看答案和解析>>
科目:高中化学 来源: 题型:
氢能是一种极具发展潜力的清洁能源。以太阳能为热源,热化学硫碘循环分解水是一种高效、无污染的制氢方法。其反应过程如下图所示:
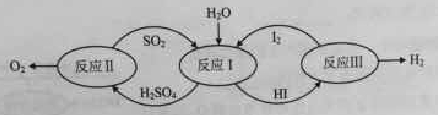
(1)反应Ⅰ的化学方程式是。
(2)反应Ⅰ得到的产物用I2进行分离。该产物的溶液在过量I2的存在下会分成两层——含低浓度I2的H2SO4层和高浓度的I2的HI层。
①根据上述事实,下列说法正确的是(选填序号)。
a.两层溶液的密度存在差异
b.加I2前,H2SO4溶液和HI溶液不互溶
c.I2在HI溶液中比在H2SO4溶液中易溶
②辨别两层溶液的方法是。
③经检测,H2SO4层中c(H+):c(SO42-)=2.06:1。其比值大于2的原因是。
(3)反应Ⅱ:2H2SO4(l)=2SO2(g)+O2(g)+2H2O(g) △H=+550kJ/mol
它由两步反应组成:i H2SO4(l)=SO3(g) +H2O(g) △H=+177kJ/mol
 ii SO3(g)分解。
ii SO3(g)分解。
L(L1、L2),X可分别代表压强或温度。下图表示L一定时,ii中SO3(g)的平衡转化率随X的变化关系。
①X代表的物理量是。
②判断L1、L2的大小关系,并简述理由:。
查看答案和解析>>
科目:高中化学 来源: 题型:
化学与生活密切相关。下列说法不正确的是( )
A.乙烯可作水果的催熟剂
B.硅胶可作袋装食品的干燥剂
C.福尔马林可作食品的保鲜剂
D.氢氧化铝可作胃酸的中和剂
查看答案和解析>>
科目:高中化学 来源: 题型:
氧化镁在医药、建筑等行业应用广泛。硫酸镁还原热解制备高纯氧化镁是一种新的探索。以菱镁矿(主要成分为MgCO3,含少量FeCO3)为原料制备高纯氧化镁的实验流程如下:

(1)MgCO3与稀硫酸反应的离子方程式为 。
(2)加入H2O2氧化时,发生反应的化学方程式为 。
(3)滤渣2的成分是 (填化学式)。
 (4)煅烧过程存在以下反应:
(4)煅烧过程存在以下反应:
2MgSO4+C 2MgO+2SO2↑+CO2↑
2MgO+2SO2↑+CO2↑
MgSO4+C MgO+SO2↑+CO↑
MgO+SO2↑+CO↑
MgSO4+3C MgO+S↑+3CO↑
MgO+S↑+3CO↑
利用右图装置对煅烧产生的气体进行分步吸收或收集。
①D中收集的气体可以是 (填化学式)。
②B中盛放的溶液可以是 (填字母)。
a.NaOH 溶液 b.Na2CO3溶液 c.稀硝酸 d.KMnO4溶液
③A中得到的淡黄色固体与热的NaOH溶液反应,产物中元素最高价态为+4,写出该反应的离子方程式: 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com