
(12分)已知Cr(OH)3在碱性较强的溶液中将生成[Cr(OH)4]―,铬的化合物有毒,由于+6价铬的强氧化性,其毒性是+3价铬毒性的100倍。因此,必须对含铬的废水进行处理,可采用以下两种方法。
Ⅰ.还原法 在酸性介质中用FeSO4等将+6价铬还原成+3价铬。
具体流程如下:

有关离子完全沉淀的pH如下表:
有关离子 | Fe2+ | Fe3+ | Cr3+ |
完全沉淀为对应氢氧化物的pH | 9.0 | 3.2 | 5.6 |
(1)写出Cr2O2- 7与FeSO4溶液在酸性条件下反应的离子方程式 。
(2)还原+6价铬还可选用以下的 试剂(填序号)。
A.明矾 B.亚硫酸氢钠 C.生石灰 D.铁屑
(3)在含铬废水中加入FeSO4,再调节pH,使Fe3+和Cr3+产生氢氧化物沉淀。
则在操作②中可用于调节溶液pH的试剂为: (填序号);
A.Na2O2 B.Ba(OH)2 C.Ca(OH)2 D.NaOH
此时调节溶液的pH范围在 (填序号)最佳。
A.3~4 B.6~8 C.10~11 D.12~14
Ⅱ.电解法 将含+6价铬的废水放入电解槽内,用铁作阳极,加入适量的氯化钠进行电解。阳极区生成的Fe2+和Cr2O2- 7发生反应,生成的Fe3+和Cr3+在阴极区与OH-结合生成Fe(OH)3和Cr(OH)3沉淀除去。
(4)写出阴极的电极反应式 。
(5)电解法中加入氯化钠的作用是 。
(12分,化学方程式缺条件或箭头只扣1分)
(1)Cr2O72― + 6 Fe2+ + 14H+=2Cr3+ + 6Fe3+ + 7H2O(2分)
(2)BD (2分,只选1个且对得1分,错选不给分)
(3)CD (2分,只选1个且对得1分,错选不给分) B(2分)
(4)2H+ + 2e―=H2↑或2H2O + 2e―=H2↑ + 2OH―(2分) (5)增强溶液导电性或盐析(2分)
【解析】
试题分析:(1)Cr2O2- 7与FeSO4溶液在酸性条件下发生氧化还原反应的离子方程式为Cr2O72― + 6 Fe2+ + 14H+=2Cr3+ + 6Fe3+ + 7H2O。
(2)A.明矾没有还原性,A错误;B.亚硫酸氢钠极易还原性,可以还原重铬酸根,B正确;C.生石灰是氧化钙,没有还原性,C错误;D.铁屑是活泼的金属,能还原重铬酸根,D正确,答案选BD。
(3)A.Na2O2具有强氧化性,能氧化硫酸亚铁,A错误;B.Ba(OH)2能与硫酸根反应生成硫酸钡沉淀,B错误;Ca(OH)2和Love,均调节pH,且能形成氢氧化物沉淀,CD正确,答案选CD。根据表中数据可知pH大于5.6时铬离子沉淀完全。又因为Cr(OH)3在碱性较强的溶液中将生成[Cr(OH)4]―,所以此时调节溶液的pH范围在6~8 最佳,答案选B。
(4)电解池中阴极得到电子发生还原反应,则阴极应该是溶液中的氢离子放电,即阴极的电极反应式为2H+ + 2e―=H2↑。
(5)氯化钠是强电解质,因此电解法中加入氯化钠的作用是增强溶液导电性。
考点:考查氧化还原反应、电化学以及物质的分离与提纯实验设计


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:2014-2015河南省濮阳市高二上学期第三次月考化学试卷(解析版) 题型:选择题
某原电池的电池反应为:Fe+2Fe3+===3Fe2+,与此电池反应不符的原电池是
A.铜片、铁片、FeCl3溶液组成的原电池
B.石墨、铁片、Fe(NO3)3溶液组成的原电池
C.铁片、锌片、Fe2(SO4)3溶液组成的原电池
D.铜片、铁片、Fe(NO3)3溶液组成的原电池
查看答案和解析>>
科目:高中化学 来源:2014-2015学年江西省景德镇市高三第二次质检理综化学试卷(解析版) 题型:选择题
某种聚合物锂离子电池放电时的反应为Li1-xCoO2+LixC6===6C+LiCoO2,其电池如图所示。下列说法不正确的是

A.放电时,LixC6发生氧化反应
B.充电时,Li+通过阳离子交换膜从左向右移动
C.充电时将电池的负极与外接电源的负极相连阳离子交换膜
D.放电时,电池的正极反应为Li1-xCoO2+xLi++xe-===LiCoO2
查看答案和解析>>
科目:高中化学 来源:2014-2015学年江苏省镇江市高三第一学期期末调研测试化学试卷(解析版) 题型:选择题
瑞典ASES公司设计的曾用于驱动潜艇的液氨—液氧燃料电池示意图如下图所示,有关说法正确的是

A.电极2发生氧化反应
B.电池工作时,Na+ 向负极移动
C.电流由电极1经外电路流向电极2
D.电极1发生的电极反应为:2NH3+6OH—-6e-=N2↑+6H2O
查看答案和解析>>
科目:高中化学 来源:2014-2015学年江苏省镇江市高三第一学期期末调研测试化学试卷(解析版) 题型:选择题
下列有关化学用语的表示正确的是
A.质量数为37的氯原子:
B.二氧化碳分子的比例模型:

C. NH4Br的电子式:
D.对羟基苯甲醛的结构简式:
查看答案和解析>>
科目:高中化学 来源:2014-2015学年江苏省苏州市高三上学期期末调研测试化学试卷(解析版) 题型:选择题
下列有关实验原理、方法和结论都正确的是
A.向饱和氯化铝溶液中滴加过量氨水可以得到NH4AlO2溶液
B.为除去BaCO3中少量的BaSO4,可用饱和碳酸钠溶液多次洗涤BaCO3
C.用冰醋酸、蒸馏水和容量瓶等可以配制pH=1的醋酸溶液
D.某溶液中滴加少量氯水后再滴加KSCN,溶液显红色,则溶液中一定含Fe2+
查看答案和解析>>
科目:高中化学 来源:2014-2015学年江苏省苏州市高三上学期期末调研测试化学试卷(解析版) 题型:选择题
设N0表示阿伏加德罗常数的值。下列说法正确的是
A.常温常压下,16 g CH4中含有的原子总数为5N0
B.标准状况下,11.2 LCH3OH中含有的共价键数目为2.5N0
C.常温常压下,2.24 L CO和CO2混合气体中含有的碳原子数目为0.1N0
D.标准状况下,0.1 mol Cl2被氢氧化钠溶液完全吸收,转移的电子数目为0.2N0
查看答案和解析>>
科目:高中化学 来源:2014-2015学年湖北省荆州市部分县市高三上学期期末统考理综化学试卷(解析版) 题型:填空题
[化学——选修5有机化学基础](15分)
某芳香烃A,分子式为C8H10;某烃类衍生物X,分子式为C15H14O3,能使FeCl3溶液显紫色;J分子内有两个互为对位的取代基。在一定条件下有如下的转化关系(无机物略去):

(1)属于芳香烃类的A的一种同分异构体(不包括A)中,在同一平面的原子最多有 个;
(2)J中所含的含氧官能团的名称为 。
(3)E与H反应的化学方程式是 ;反应类型是 。
(4)B、C的混合物在NaOH乙醇溶液中加热可以生成同一种有机物M,以M为单体合成的高分子化合物的名称是
(5)已知J有多种同分异构体,写出一种符合下列性质的J的同分异构体的结构简式:
①与FeCl3溶液作用显紫色;
②与新制Cu(OH)2悬浊液作用产生红色沉淀;
③苯环上的一卤代物有2种。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年福建省泉州市高三上学期期末化学试卷(解析版) 题型:简答题
(11分)LiAlH4由Li+、A1H4一构成,是有机合成中常用的还原剂。
(1)Al元素在周期表的位置是第__________周期__________族。
(2)比较离子半径大小:Li+__________ H一(选填“>"、“<”或“=”)。
(3)LiAlH4中含有的化学键类型为____________________________________。
(4)LiAlH4中氢元素的化合价为__________,它与水反应生成的单质气体为__________。
(5)LiCl溶液显酸性,用离子方程式说明原因____________________________________。
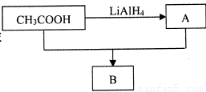
(6)如图所示,已知75%A的水溶液常用于医疗消毒,则A的结构简式为__________;CH3COOH与A在浓硫酸催化下生成B的有机反应类型为__________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com