
物质的结构决定性质,性质反映其结构特点。
(1)金刚石和石墨是碳元素的两种常见单质,下列叙述中正确的有
a.金刚石中碳原子的杂化类型为sp3杂化,石墨中碳原子的杂化类型为sp2杂化;
b.晶体中共价键的键长:金刚石中C—C<石墨中C—C;
c.晶体的熔点:金刚石< 石墨
d.晶体中共价键的键角:金刚石>石墨
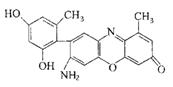 (2)某石蕊的分子结构如右图所示。
(2)某石蕊的分子结构如右图所示。
①石蕊分子所含元素中,基态原子2p轨道有两个成单电子的是 (填元素符号); 由其中两种元素形成的三角锥构型的一价阳离子是 (填化学式);
②该石蕊易溶解于水,分析可能的原因是 ;
(3)铜及其合金是人类最早使用的金属材料。
①NF3可由NH3和F2在Cu催化剂存在下反应直接得到:4NH3+3F2 NF3+3NH4F
NF3+3NH4F
 上述化学方程式中的5种物质所属的晶体类型有_______(填序号)。
上述化学方程式中的5种物质所属的晶体类型有_______(填序号)。
a.离子晶体 b.分子晶体 c.原子晶体 d.金属晶体
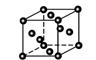
②金属铜采取如图所示堆积方式,可称为_____堆积,则Cu晶体中
Cu原子的配位数为
科目:高中化学 来源: 题型:
关于化学键的叙述中,正确的是( )
A.离子化合物可能含共价键 B.共价化合物可能含离子键
C.离子化合物中只含离子键 D.离子化合物中一定含有金属离子
查看答案和解析>>
科目:高中化学 来源: 题型:
有A、B、C、D、E五种元素,元素A的一种原子无中子,元素B和C都有2个电子层,它们能生成无色无嗅的气体BC2,元素D有三个电子层,它和元素C属于同一主族,D和C生成有刺激性气味的气体DC2;元素E的阳离子E+的电子层结构与Ar的电子层结构相同,试回答:
(1)它们的元素符号是:
A B C D (2分每空)
(2)(3分)A和D的化合物与C和D的化合物(DC2)能否反应?若能反应写出反应方程式: ,
(3) 。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列图示与对应的叙述相符的是
A.图Ⅰ中 可以看出反应A(g)=C(g)的△H=(E1-E4)kJ·mol-1
B.图Ⅱ表示一定条件下进行的反应2SO2+O2 2SO3 各成分的物质的量变化,t2时刻改变的条件可能是扩大了容器的体积
2SO3 各成分的物质的量变化,t2时刻改变的条件可能是扩大了容器的体积
C.图Ⅲ表示将CO2通入NaOH的稀溶液中,随着CO2的通入,溶液中水电离出的c(H+)变化关系
D.图Ⅳ曲线表示用0.1000mol/LNaOH溶液分别滴定浓度相同的三种一元酸,由此可判断HX的酸性最强
查看答案和解析>>
科目:高中化学 来源: 题型:
将铁片和银片用导线连接置于同一稀盐酸溶液中,并经过一段时间后,下列叙述正确的
A.负极有Cl2逸出,正极有H2逸出 B.负极附近Cl-的浓度减小
C.正极附近Cl-的浓度逐渐增大 D.溶液中Cl-的浓度基本不变
查看答案和解析>>
科目:高中化学 来源: 题型:
在372K时,把0.5molN2O4通入体积为5L的真空密闭容器中,立即出现红棕色。反应进行到2s时,NO2的浓度为0.02mol/L。在60s时,体系达到平衡,此时容器内的压强为开始时压强的1.6倍。下列说法正确的是 高 考 资 源 网
A 前2s 以N2O4浓度变化表示的平均反应速率为0.01mol/(L.S)
B 在2s时体系内的压强为开始时的1.1倍
C 在平衡体系内含有N2O4 0.25mol D 平衡时N2O4的转化率为60%
查看答案和解析>>
科目:高中化学 来源: 题型:
恒温下,反应aX(g)  bY(g) + cZ(g),达到平衡状态。若把容器的体积压缩到原来的
bY(g) + cZ(g),达到平衡状态。若把容器的体积压缩到原来的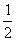 ,达到平衡状态时,X的物质的量浓度从0.1mol/L增大到0.19mol/L。下列判断正确的是( )
,达到平衡状态时,X的物质的量浓度从0.1mol/L增大到0.19mol/L。下列判断正确的是( )
A.a>b+c B.a=b+c C.a<b+c D.a=b=c
查看答案和解析>>
科目:高中化学 来源: 题型:
能说明氯的非金属性比硫强的事实是
A.氯气与氢气反应生成氯化氢,而硫与氢气反应生成硫化氢
B.向硫化氢的水溶液中通入氯气可得到淡黄色的硫
C.氯气能与水反应而硫不能
D.氯原子最外电子层上有7个电子而硫最外电子层上有6个电子
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com