
(8��) CO2������Ҫ��������,��ν��ʹ�����CO2�ĺ�������Ч�ؿ�������CO2�����ش����塣
��1����ѧ����H2��CO2�����״�ȼ�ϡ�Ϊ̽���÷�Ӧԭ������������ʵ�飺ij�¶��£����ݻ�Ϊ2 L���ܱ������г���1 mol CO2��3��25 mol H2����һ�������·�Ӧ�����CO2��CH3OH(g)��H2O(g)�����ʵ���(n)��ʱ��ı仯��ϵ��ͼ��ʾ��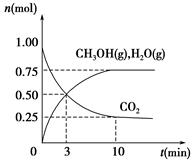
��д���÷�Ӧ�Ļ�ѧ����ʽ_______________________ ����ӷ�Ӧ��ʼ��3 minʱ��������ƽ����Ӧ����v(H2)��____________________��
�����д�ʩ��һ����ʹCO2��ת�����������___________________ ��
A ��ԭ�������ٳ���1 mol H2 B ��ԭ�������ٳ���1 mol CO2
C ��С�������ݻ� D ʹ�ø���Ч�Ĵ���
E����ԭ�����г���1 mol He F����ˮ��������ϵ�з����
��2����ѧ�һ�����������һ���������������̼��Ӧ�����Ҵ�ȼ�ϣ����Ȼ�ѧ��Ӧ����ʽΪ:2CO2(g)��6H2(g)  CH3CH2OH(g)��3H2O(g)����H��a kJ��mol��1��
CH3CH2OH(g)��3H2O(g)����H��a kJ��mol��1��
��3����һ��ѹǿ�£���ø÷�Ӧ��ʵ�����������ʾ������ݱ������ݻش��������⡣
 �¶�(K) �¶�(K) CO2ת����/(%) CO2ת����/(%)n(H2)/n(CO2) | 500 | 600 | 700 | 800 |
| 1��5 | 45 | 33 | 20 | 12 |
| 2 | 60 | 43 | 28 | 15 |
| 3 | 83 | 62 | 37 | 22 |
 ��ֵ��CO2ת����_________�������Ҵ������ʵ���________(���������С���������䡱����ȷ����)��
��ֵ��CO2ת����_________�������Ҵ������ʵ���________(���������С���������䡱����ȷ����)�� ��1�� �� CO2 ��3H2 CH3OH ��H2O ��0��375 mol��L��1��min��1����A��C��F��
CH3OH ��H2O ��0��375 mol��L��1��min��1����A��C��F��
��2�� ��С�� ���ڲ��� ������������
���������������1���ٸ�������ɵø÷�Ӧ�Ļ�ѧ����ʽ��CO2 ��3H2  CH3OH ��H2O��V(CO2)=(1��00-0��25)mol��2L��3min=0��125mol/(L��min),V(H2)="3" V(CO2)=0��375mol/(L��min), ��A������Ӧ���Ũ�ȿ���ʹƽ�������ƶ�����˿������CO2��ת���ʣ���ȷ��B����ԭ�������ٳ���1 mol CO2,ƽ�������ƶ�������ƽ���ƶ�������ԶС�ڼ����������CO2��ת���ʷ������ͣ�����C����С�������ݻ���������ѹǿ��ƽ�������������С�ķ���������Ӧ�����ƶ����ʿ������CO2��ת���ʣ���ȷ��D��ʹ�ø���Ч�Ĵ��������Լӿ췴Ӧ���ʣ����Dz���ʱƽ���ƶ���CO2��ת���ʲ��䣬����E����ԭ�����г���1 mol He�����ڷ�Ӧ������и���ֵ�Ũ�Ȳ��䣬����ƽ�ⲻ�����ƶ�������F����ˮ��������ϵ�з���������С���������Ũ�ȣ�ƽ�������ƶ�����˿������CO2��ת���ʣ���ȷ����2�����ڼ������ʵ����ı���ͬʱ�����������¶ȣ�CO2ת���ʽ��ͣ�˵�������¶ȣ�ƽ�������ƶ�������ƽ���ƶ�ԭ���������¶ȣ�ƽ�������ȷ�Ӧ�����ƶ����淴Ӧ���������ȷ�Ӧ�����Ը÷�Ӧ������Ӧ�Ƿ��ȷ�Ӧ�����������Ӧ��a<0�� �ں����£���Ӧ��ϵ�м��������������¶Ȳ��䣬��÷�Ӧ�ķ�Ӧ��aֵ���䣬����һ���¶��£�����
CH3OH ��H2O��V(CO2)=(1��00-0��25)mol��2L��3min=0��125mol/(L��min),V(H2)="3" V(CO2)=0��375mol/(L��min), ��A������Ӧ���Ũ�ȿ���ʹƽ�������ƶ�����˿������CO2��ת���ʣ���ȷ��B����ԭ�������ٳ���1 mol CO2,ƽ�������ƶ�������ƽ���ƶ�������ԶС�ڼ����������CO2��ת���ʷ������ͣ�����C����С�������ݻ���������ѹǿ��ƽ�������������С�ķ���������Ӧ�����ƶ����ʿ������CO2��ת���ʣ���ȷ��D��ʹ�ø���Ч�Ĵ��������Լӿ췴Ӧ���ʣ����Dz���ʱƽ���ƶ���CO2��ת���ʲ��䣬����E����ԭ�����г���1 mol He�����ڷ�Ӧ������и���ֵ�Ũ�Ȳ��䣬����ƽ�ⲻ�����ƶ�������F����ˮ��������ϵ�з���������С���������Ũ�ȣ�ƽ�������ƶ�����˿������CO2��ת���ʣ���ȷ����2�����ڼ������ʵ����ı���ͬʱ�����������¶ȣ�CO2ת���ʽ��ͣ�˵�������¶ȣ�ƽ�������ƶ�������ƽ���ƶ�ԭ���������¶ȣ�ƽ�������ȷ�Ӧ�����ƶ����淴Ӧ���������ȷ�Ӧ�����Ը÷�Ӧ������Ӧ�Ƿ��ȷ�Ӧ�����������Ӧ��a<0�� �ں����£���Ӧ��ϵ�м��������������¶Ȳ��䣬��÷�Ӧ�ķ�Ӧ��aֵ���䣬����һ���¶��£����� ��ֵ������������һ�ַ�Ӧ���Ũ�ȣ�����ʹ�������ʵ�ת���������CO2ת������������ƽ�������ƶ������������Ҵ������ʵ�������
��ֵ������������һ�ַ�Ӧ���Ũ�ȣ�����ʹ�������ʵ�ת���������CO2ת������������ƽ�������ƶ������������Ҵ������ʵ�������
���㣺���黯ѧ��Ӧ���ʵļ��㡢�������ת���ʵĴ�ʩ����Ӧ�ȵ��жϵ�֪ʶ��


 ��ĩ���100�ִ��½����ȫ�Ծ�ϵ�д�
��ĩ���100�ִ��½����ȫ�Ծ�ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
�ں��º�ѹ�£����ܱ������г���4mol A��2 mol B���������·�Ӧ��2A(g)+B(g) 2C(g)�� ��H��0��2min��Ӧ�ﵽƽ�⣬����CΪ1.6mol�������з�����ȷ���� �� ��
2C(g)�� ��H��0��2min��Ӧ�ﵽƽ�⣬����CΪ1.6mol�������з�����ȷ���� �� ��
A.����Ӧ��ʼʱ�������Ϊ2L����Vc��0.4mol?L-1?min-1
B.���ں�ѹ���������·�Ӧ��ƽ���nc����1.6mol
C.��2min������������Ͷ������ʵ���A��C��B��ת���ʲ���
D.���÷�Ӧ�ں��º����½��У��ų�����������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
(10��) ���о����������������ڴ����к������ӵ������ʱ���漰���·�Ӧ��
2NO2��g��+NaCl��s�� NaNO3��s��+ClNO��g�� K1 ?H < 0 ��I��
NaNO3��s��+ClNO��g�� K1 ?H < 0 ��I��
2NO��g��+Cl2��g�� 2ClNO��g�� K2 ?H < 0 ��II��
2ClNO��g�� K2 ?H < 0 ��II��
��1��4NO2��g��+2NaCl��s��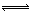 2NaNO3��s��+2NO��g��+Cl2��g����ƽ�ⳣ��K= ����K1��K2��ʾ����
2NaNO3��s��+2NO��g��+Cl2��g����ƽ�ⳣ��K= ����K1��K2��ʾ����
��2��Ϊ�о���ͬ�����Է�Ӧ��II����Ӱ�죬�ں��������£���2L�����ܱ������м���0.2mol NO��0.1mol Cl2��10minʱ��Ӧ��II���ﵽƽ�⡣���10min��v��ClNO��=7.5��10-3mol?L-1?min-1����ƽ���n��Cl2��= mol��NO��ת���ʧ�1= �������������ֲ��䣬��Ӧ��II���ں�ѹ�����½��У�ƽ��ʱNO��ת���ʧ�2 ��1���>����<����=������ƽ�ⳣ��K2 ���������С�����䡱����ҪʹK2��С���ɲ��õĴ�ʩ�� ��
��3����֪t��ʱ����ӦFeO(s)��CO(g) Fe(s)��CO2(g)��ƽ�ⳣ��K��0.25��
Fe(s)��CO2(g)��ƽ�ⳣ��K��0.25��
��t��ʱ����Ӧ�ﵽƽ��ʱn(CO)��n(CO2)�� ��
������1 L�ܱ������м���0.02 mol FeO(s)����ͨ��xmolCO��t��ʱ��Ӧ�ﵽƽ�⡣��ʱFeO(s)ת����Ϊ50%����x�� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
��5�֣�H2���Դ���ԭNO�Դﵽ������Ⱦ��Ŀ�ģ�
��1����֪����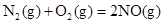
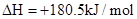
��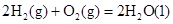
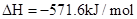
��H2��g����NO��g����Ӧ����N2��g����H2O��l�����Ȼ�ѧ����ʽΪ��________________��
��2��һ�������£������Ϊ2 L��������ͨ��1 mol H2��l mol NO��������N2��g����H2O��l�����÷�Ӧ��ƽ��ʱ�������ڵ�ѹǿ�Ƿ�Ӧ��ʼʱ��40�������������������䣬ֻ����������ͨ��1 mol H2�����㷴Ӧ�ٴ���ƽ��ʱ����ѧƽ�ⳣ��Ϊ__________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
��10�֣�800�桢2L�ܱ�������Ӧ2NO(g)��O2(g) 2NO2(g)��ϵ�У� n(NO)��
2NO2(g)��ϵ�У� n(NO)��
ʱ��ı仯�����
| ʱ�䣨s�� | 0 | 1 | 2 | 3 | 4 | 5 |
| n(NO)(mol) | 0.020 | 0.010 | 0.008 | 0.007 | 0.007 | 0.007 |
 ��3�� ��Ӧ�ﵽƽ��״̬ʱNO��ת����= ������ʾ �� ��
��3�� ��Ӧ�ﵽƽ��״̬ʱNO��ת����= ������ʾ �� ���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
(14��)�ҹ��зḻ����Ȼ����Դ������Ȼ��Ϊԭ�Ϻϳ����ص���Ҫ��������ͼ��ʾ��ͼ��ijЩת��
���輰������δ�г�����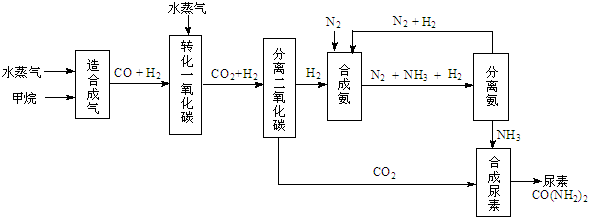
��1������ϳ������������Ȼ�ѧ����ʽ��CH4(g)+H2O(g)  CO(g)+3H2(g)����H��0
CO(g)+3H2(g)����H��0
�ں��º��ݵ������£������CH4�ķ�Ӧ���ʺ�ת���ʣ����д�ʩ���е��� ��
A������ѹǿ B�������¶� C������He�� D������ˮ����Ũ��
| �¶�/�� | 400 | 500 | 800 |
| ƽ�ⳣ��K | 9.94 | 9 | 1 |
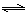 H2(g)+CO2(g)���÷�Ӧƽ�ⳣ�����¶ȵı仯���£�
H2(g)+CO2(g)���÷�Ӧƽ�ⳣ�����¶ȵı仯���£��鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
��֪��N2O4(g)  2NO2(g) ��H="+57.20kJ" �� mol-1
2NO2(g) ��H="+57.20kJ" �� mol-1
��100��ʱ����0.100molN2O4�������1L���ݳ�յ��ܱ������У�ÿ��һ��ʱ��Ը������ڵ�����Ũ�Ƚ��з����õ��±����ݣ�
| ʱ�䣨s�� | 0 | 20 | 40 | 60 | 80 |
| c(N2O4) /mol����L-1 | 0.100 | c1 | 0.050 | c3 | c4 |
| c(NO2) /mol��L-1 | 0.000 | 0.060 | c2 | 0.120 | 0.120 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
(6��)��3 mol A��3 mol B�����2 L���ܱ������У��������·�Ӧ��
3A(g)+B(g)  xC(g)+2D(g)����5 min���D��Ũ��Ϊ0.5 mol��L��C��ƽ����Ӧ����Ϊ0.1 mol��(L��min)������
xC(g)+2D(g)����5 min���D��Ũ��Ϊ0.5 mol��L��C��ƽ����Ӧ����Ϊ0.1 mol��(L��min)������
��1��B��ƽ����Ӧ����Ϊ ��
��2��x��ֵΪ ��
��3��5 min��A��B�����ʵ���֮��Ϊ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
��15�֣�̼���仯�����й㷺����;��
��1���ڵ绯ѧ�У�����̼���缫���ڼ���п�̸ɵ���У�̼���� ����
��2����ˮ����ͨ�����ȵ�̼���ɲ���ˮú������ӦΪ��C��s��+H2O��g��=CO��g��+H2��g������H=+131.3kJ?mol-1����Ҫ�Ʊ���״����22.4��ˮú����ת�Ƶĵ��ӵ����ʵ���Ϊ ����Ҫ���յ�����Ϊ kJ��
(3����ҵ�ϰ�ˮú���еĻ�����徭��������õĽϴ�H2���ںϳɰ���
N2��g����3H2��g�� 2NH3��g������H=-92.4kJ?mol-1����ͼ1�������ֲ�ͬʵ��������ģ�⻯����������ʵ�������N2��ʱ��仯ʾ��ͼ��
2NH3��g������H=-92.4kJ?mol-1����ͼ1�������ֲ�ͬʵ��������ģ�⻯����������ʵ�������N2��ʱ��仯ʾ��ͼ��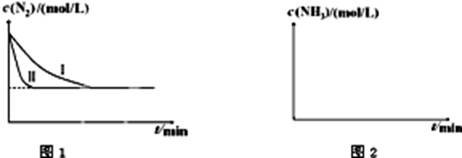
����ʵ���Ƚϣ�ʵ���ı������Ϊ�� ��
��ʵ����ʵ�����¶�Ҫ�ߣ�����������ͬ��������ͼ2�л���ʵ����ʵ�����NH3Ũ����ʱ��仯��ʾ��ͼ��
��4��Na2CO3���ڽ������������ŷ�������CO2�IJ�����1L0.2mol/L Na2CO3��Һ���ձ�״����2.24LCO2����Һ�и�����Ũ���ɴ�С��˳��Ϊ ��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com