
在允许加热的条件下,只用一种试剂就可以鉴别氯化钾、碳酸钾、偏铝酸钾、氢氧化钾、氢氧化钡、氯化钡6种溶液,这种试剂是( )
A.H2SO4 B.(NH4)2SO4
C.NH3·H2O D.NH4HSO4
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
常温下,0.01 mol·L-1 MOH溶液的pH为10。已知:2MOH(aq)+H2SO4(aq)===M2SO4(aq)+2H2O(l) ΔH1=-2 4.2 kJ·mol-1;H+(aq)+OH-(aq)===H2O(l) ΔH2=-57.3 kJ·mol-1。则MOH在水溶液中电离的ΔH为( )
4.2 kJ·mol-1;H+(aq)+OH-(aq)===H2O(l) ΔH2=-57.3 kJ·mol-1。则MOH在水溶液中电离的ΔH为( )
A.+33.1 kJ·mol-1 B.+45.2 kJ·mol-1
C.-81.5 kJ·mol-1 D.-33.1 kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
下列离子方程式表达正确的是( )
A.氢氧化铁溶于氢碘酸:Fe(OH)3+3H+===Fe3++3H2O
B.小苏打溶液呈碱性的原因:HCO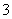 +H2OH3O++CO
+H2OH3O++CO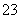
C.溴化亚铁溶液中通入足量氯气:2Fe2++4Br-+3Cl2===2Fe3++2Br2+6Cl-
D.向硫酸铝铵溶液中滴加少量Ba(OH)2溶液:NH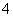 +Al3++2SO
+Al3++2SO +2Ba2++5OH-===AlO
+2Ba2++5OH-===AlO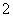 +2BaSO4↓+NH3·H2O+2H2O
+2BaSO4↓+NH3·H2O+2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
观察下图中物质分子的比例模型及其变化,请回答下列问题:
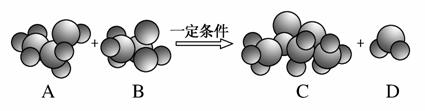
(1)A是乙醇,则B、C的结构简式分别为__________________、__________________。
(2)上图所示化学方程式中的“一定条件”是________________________________________________________________________。
(3)反应物中只有乙醇分子中的氧原子是18O,生成物中含这种氧原子的是(写物质名称)________。
(4)在B的分子中,最外层电子数为8的原子有________个。
查看答案和解析>>
科目:高中化学 来源: 题型:
有机物甲在一定条件下能发生水解反应生成两种有机物,乙中①~⑥是标出的该有机物分子中不同的化学键,在水解时,断裂的键是( )
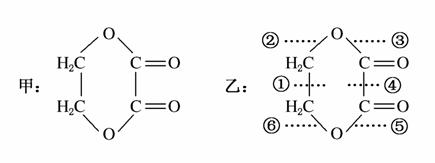
A.①④ B.③⑤
C.②⑥ D.②⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
食盐是日常生活的必需品,也是重要的化工原料。粗食盐常含有少量K+、Ca2+、Mg2+、Fe3+、SO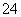 等杂质离子,实验室提纯NaCl的流程如下:
等杂质离子,实验室提纯NaCl的流程如下:

提供的试剂:饱和Na2CO3溶液、饱和K2CO3溶液、NaOH溶液、BaCl2溶液、Ba(NO3)2溶液、75%乙醇、四氯化碳
(1)欲除去溶液Ⅰ中的Ca2+、Mg2+、Fe3+、SO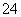 ,选出a所代表的试剂,按滴加顺序依次为____________(只填化学式)。
,选出a所代表的试剂,按滴加顺序依次为____________(只填化学式)。
(2)用于沉淀的试剂需过量,判断除去SO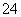 的试剂过量的方法是________________。
的试剂过量的方法是________________。
(3)洗涤除去NaCl晶体表面附带的少量KCl,选用的试剂为
________________________________________________________________________
________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
为除去MgCl2酸性溶液中的Fe3+,可在加热搅拌的条件下加入一种试剂,过滤后,向滤液中加入适量盐酸,这种试剂是 ( )
A.NH3·H2O B.NaOH
C.Na2CO3 D.MgCO3
查看答案和解析>>
科目:高中化学 来源: 题型:
银铜合金广泛用于航空工业。从切割废料中回收银并制备铜化工产品的工艺如下:
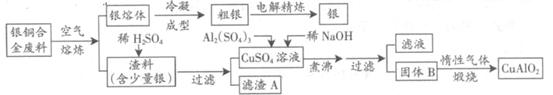
(注:Al(OH)3和Cu(OH)2开始分解的温度分别为450℃和80℃)
(1)电解精炼银时,阴极反应式为 ;滤渣A与稀HNO3反应,产生的气体在空气中迅速变为红棕色,该气体变色的化学方程式为 。
(2)固体混合物B的组成为 ;在生成固体B的过程中,需控制NaOH的加入量,若NaOH过量,则因过量引起的反应的离子方程式为 。
(3)完成煅烧过程中一个反应的化学方程式: CuO+ Al2O3 CuAlO2 + ↑。
CuAlO2 + ↑。
(4)若银铜合金中铜的质量分数为63.5%,理论上5.0kg废料中的铜可完全转化为 mol CuAlO2,至少需要1.0mol•L—1的Al2(SO4)3溶液 L。
(5)CuSO4溶液也可用于制备胆矾,其基本操作是 、过滤、洗涤和干燥。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com