
| A、KOH溶液和AlCl3溶液 |
| B、Na2CO3溶液和盐酸 |
| C、NaHCO3溶液和NaOH溶液 |
| D、盐酸和NaAlO2溶液 |


科目:高中化学 来源: 题型:
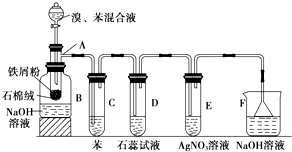 已知苯、溴和溴苯的物理性质如下表所示
已知苯、溴和溴苯的物理性质如下表所示| 苯 | 溴 | 溴苯 | |
| 密度/g?cm-3 | 0.88 | 3.10 | 1.50 |
| 沸点/℃ | 80 | 59 | 156 |
| 水中溶解度 | 微溶 | 微溶 | 微溶 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Na2O2具有漂白性 |
| B、均与水反应生成NaOH,因而均是碱性氧化物 |
| C、Na2O中氧-2价,Na2O2中氧-1价 |
| D、均可与H2O、CO2反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
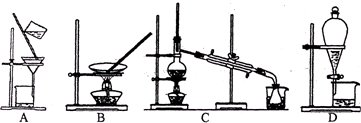
| A、集气瓶、水槽、药匙、量筒、玻璃棒 |
| B、托盘天平、大试管、玻璃棒、胶头滴管 |
| C、烧杯、容量瓶、玻璃棒、量筒、胶头滴管 |
| D、烧瓶、量筒、胶头滴管、玻璃棒、烧杯 |
查看答案和解析>>
科目:高中化学 来源: 题型:

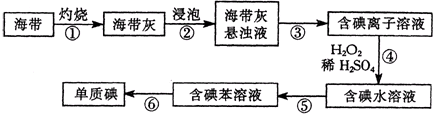
| A、从海水中提取物质都必须通过化学反应才能实现 |
| B、第②步属于物理变化 |
| C、从第④~⑤步的目的是浓缩、富集溴单质 |
| D、第①步中除去粗盐中的SO42-、Ca2+、Mg2+、Fe3+等杂质,加入试剂的顺序为:Na2CO3溶液→NaOH溶液→BaCl2溶液→过滤后加盐酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、用物质A表示的反应速率为1.2 mol/(L?s) |
| B、2 s时物质A的转化率为30% |
| C、用物质B表示的反应速率为0.6 mol/(L?s) |
| D、2 s时物质B的浓度为0.6 mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Na+、MnO4-、K+、NO3-、SO32- |
| B、Na+、CO32-、Cl-、Al3+、NO3- |
| C、Na+、S2-、OH-、K+、Cl-、NO3- |
| D、Fe2+、H+、Na+、Ca2+、NO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 1 |
| 2 |

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com