
(1)类比法是化学学习中常用的方法,已知硝酸能把铁氧化成Fe(NO3)3,但当铁过量时,产物是Fe(NO3)2。某同学受此启发,提出一个相似的观点:氯气与铁粉反应,当Cl2足量时生成FeCl3,当铁粉过量时产物是FeCl2,为了验证该观点是否正确,该同学将一定量的铁粉与Cl2恰好完全反应得到一固体物质,然后通过实验确定其成分。探究过程如下:
①提出假设:
假设1:该固体物质是FeCl2
假设2:该固体物质是FeCl3
 假设3:该固体物质是__________________。
假设3:该固体物质是__________________。
②设计实验方案:
取少量固体物质于烧杯中,加适量水溶解,得到溶液A,然后取两份A溶液分别进行实验,实验现象与结论如下表:
| 实验方法 | 实验现象 | 结 |
| 在溶液中加KSCN溶液 | 固体物质中有FeCl3 | |
| 在KMnO4溶液中加少量A溶液 | KMnO4溶液颜色无明显变化 | 固体物质中不含________ |
③根据上述实验结论,写出Cl2与铁粉加热时反应的化学方程式_________________。
(2)为了进一步探究FeCl3溶液的性质,该同学又利用A溶液作了如下一些实验,其中正确的是________。
A.将A溶液滴入沸水中,并继续加热得到红褐色液体,该液体能产生丁达尔现象
B.在A溶液中加入淀粉KI溶液,溶液变蓝
C.在A溶液中滴加NaOH浓溶液,出现红褐色沉淀
D.在A溶液中加入Fe、Cu固体后,充分反应后剩余固体中不可能有Fe无Cu
E.将A溶液加热蒸干并灼烧,得到FeCl3固体
(3)电子工业常用30%的FeCl3溶液腐蚀敷在绝缘板上的铜箔,制造印刷电路板。某工程师为了从废液中回收铜,重新获得FeCl3溶液,设计了下列实验步骤: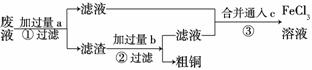
写出一个能证明还原性Fe比Cu强的 离子方程式:________
离子方程式:________ _______________________
_______________________
________________________________________________________________________。该反应在上图步骤
________中发生。请根据上述反应设计一个原电池,在方框中画出简易装置图(标出电极名称、电极材料、电解质溶液)。

上述过程回收的铜是粗铜,为了获得更纯的铜必须进行电解精炼。写出电解精炼时阳极材料及主要的电极反应式________________________________________________
_______________________________________________________ _________________。
_________________。
解析:(1)与硝酸在不同条件下可被氧化成两种产物,推断铁粉与Cl2反应也可能生成FeCl2或FeCl3或两种物质的混合物。根据KSCN溶液能与Fe3+显红色,可检验产物中是否含有FeCl3。根据酸性KMnO4溶液能氧化Fe2+而褪色,可验证产物中是否含有FeCl2。
(2)FeCl3滴入沸水中,继续煮沸可生成Fe(OH)3胶体,有丁达尔现象。Fe3+能氧化I-生成I2,Fe3+能与NaOH溶液生成Fe(OH)3红褐色沉淀。而加热蒸干FeCl3溶液,由于Fe3+的水解,会生成Fe(OH)3沉淀,经灼烧,得到Fe2O3,而不是FeCl3固体。在FeCl3溶液中加入Fe、Cu固体后,发生以下反应:Fe+2Fe3+===3Fe2+,Cu+2Fe3+===Cu2++2Fe2+,Fe+Cu2+===Cu+Fe2+。由此看出剩余固体中不可能有Fe无Cu,而只能是Cu或Cu、Fe混合物。
(3)废液中回收铜的实验过程如下:
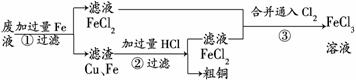
Fe能从CuCl2溶液中置换出铜,可证明Fe比Cu的还原性强,反应方程式为:Fe+Cu2+===Fe2++Cu。用原电池表示该反应时,可用Fe作负极,Cu作正极,CuCl2溶液作电解质溶液。电解精炼铜时,粗铜作阳极(Cu-2e-===Cu2+),纯铜作阴极(Cu2++2e-===Cu),含Cu2+的溶液作电解质溶液。
答案:(1)①FeCl2和FeCl3 ②溶液呈红色 FeCl2
③2Fe+3Cl2 2FeCl3
2FeCl3
(2)A、B、C、D
(3)Fe+Cu2+===Fe2++Cu ①

粗铜 Cu-2e-===Cu2+


 口算心算速算应用题系列答案
口算心算速算应用题系列答案 同步拓展阅读系列答案
同步拓展阅读系列答案科目:高中化学 来源: 题型:
已知某温度下CH3COOH和NH3·H2O的电离常数相等,现向10 mL浓度为0.1 mol·L-1的CH3COOH溶液中滴加相同浓度的氨水,在滴加过程中( )
A.水的电离程度始终增大
B. 先增大再减小
先增大再减小
C.c(CH3COOH)与c(CH3COO-)之和始终保持不变
D.当加入氨水的体积为10 mL时,c(NH )=c(CH3COO-)
)=c(CH3COO-)
查看答案和解析>>
科目:高中化学 来源: 题型:
25 ℃时,下列各组离子在指定溶液中一定能大量共存的是( )
A.pH=1的溶液中:Na+、K+、MnO 、CO
、CO
B.c(H+)=1×10-13 mol·L-1的溶液中:Mg2+、Cu2+、SO 、NO
、NO
C.0.1 mol·L-1NH4HCO3溶液中:K+、Na+、NO 、Cl-
、Cl-
D.0.1 mol·L-1FeCl3溶液中:Fe2+、NH 、SCN-、SO
、SCN-、SO
查看答案和解析>>
科目:高中化学 来源: 题型:
氧化还原反应与四种基本反应类型的关系如下图所示,则下列化学反应属于阴影3区域的是( )

A.Cl2+2NaI===2NaCl+I2
B.NH4HCO3 NH3↑+H2O+CO2↑
NH3↑+H2O+CO2↑
C.4Fe(OH)2+O2+2H2O===4Fe(OH)3
D.Fe2O3+3CO 2Fe+3CO2
2Fe+3CO2
查看答案和解析>>
科目:高中化学 来源: 题型:
反应①是自海藻灰中提取碘的主要反应,反应②是自智利硝石中提取碘的主要反应
①2NaI+MnO2+3H2SO4=== 2NaHSO4+MnSO4+2H2O+I2
②2NaIO3+5NaHSO3===2Na2SO4+3NaHSO4+H2O+I2
已知NaIO3的氧化性与MnO2相近,下列有关说法正确的是( )
A.I2在反应①中是氧化产物,在反应②中是还原产物
B.两个反应中生成等量的I2时转移的电子数相等
C.NaI和NaIO3在一定条件下能反应生成I2
D.NaIO3在 化学反应中只能做氧化剂不能做还原剂
化学反应中只能做氧化剂不能做还原剂
查看答案和解析>>
科目:高中化学 来源: 题型:
欲从苯酚的乙醇溶液中回收苯酚,有下列操作:
①蒸馏;②过滤;③分液;④加入足量的钠;⑤通入过量的CO2;⑥加入足量的NaOH溶液;⑦加入足量的FeCl3溶液;⑧加入乙醇和浓硫酸的混合液;⑨加入足量的浓溴水;⑩加入适量盐酸。
合理的步骤是( )
A.④⑤⑩ B.⑥①⑤③
C.⑨②⑧① D.⑦①③⑩
查看答案和解析>>
科目:高中化学 来源: 题型:
2008年北京奥运会对兴奋剂采取了严格的检验措施,最大限度地控制了运动员服用兴奋剂现象的出现。某种兴奋剂的结构简式如下图所示:

回答下列问题:
(1)该物质最多有________个碳原子共平面,它与苯酚_______(填“是”或“不是”)同系物,理由是_____________________________
___________________________________________________________________________________________________________________。
(2)该兴奋剂与FeCl3溶液混合,现象是________。
(3)滴入KMnO4酸性溶液,振荡,紫色褪去,________(填“能”或“不能”)证明其结构中含有碳碳双键,理由是______________。
(4)1 mol 该物质分别与浓溴水和H2反应时最多消耗Br2和H2分别为________mol和________mol。
查看答案和解析>>
科目:高中化学 来源: 题型:
一定条件下,可逆反应N2 + 3H2 2NH3达到化学平衡状态,下列说法一定正确的是( )
2NH3达到化学平衡状态,下列说法一定正确的是( )
A.每1 mol N≡N断裂的同时有2 mol N—H生成
B.N2、H2、NH3的浓度之比为1:3:2
C.N2减少的速率和NH3减少的速率之比为1:2
D.气体体积为初始体积的
查看答案和解析>>
科目:高中化学 来源: 题型:
 A是一种重要的化工原料,已知A是一种卤代烃,,相对分子质量为92.5,其核磁共振氢谱中只有一个峰,C是一种高分子化合物,M是一种六元环状酯,转化关系如图所示,回答下列问题:
A是一种重要的化工原料,已知A是一种卤代烃,,相对分子质量为92.5,其核磁共振氢谱中只有一个峰,C是一种高分子化合物,M是一种六元环状酯,转化关系如图所示,回答下列问题:
(1)A的分子式 ;A→B的反应类型 ;
(2)写出结构简式:D ,M 。
(3)写出下列反应的化学方程式:
B→C: ;E→F: 。
(4)满足下列条件的H的同分异构体有 种。写出其中一种同分异构体的结构简
式 。
①属于酯类; ②能发生银镜反应; ③能与金属钠反应放出气体。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com