
| A、①③⑤ | B、①②③⑥ |
| C、①②③④⑤ | D、①②③④⑤⑥ |


科目:高中化学 来源: 题型:
| A、6.85倍 | B、9倍 |
| C、11.5倍 | D、17.8倍 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、AlCl3和NaOH |
| B、NaOH和HCl |
| C、NaHCO3和HCl |
| D、NaCl和AgNO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、根据红外光谱图的分析可以初步判断有机物中具有哪些基团 |
| B、实验室制乙炔的反应是氧化还原反应 |
| C、“神州七号”的防护层中含聚四氟乙烯,聚四氟乙烯属于不饱和烃 |
| D、用酸性高锰酸钾溶液除去乙炔中含有的H2S |
查看答案和解析>>
科目:高中化学 来源: 题型:
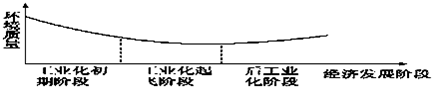
| A、环境污染不可避免,只能采取“先污染,后治理”的策略 |
| B、后工业化阶段环境问题会自然解决 |
| C、保护环境至关重要,必须杜绝兴建产生污染的工业设施 |
| D、应当采取措施减少或避免发展过程中的环境污染问题 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| ||
| ||
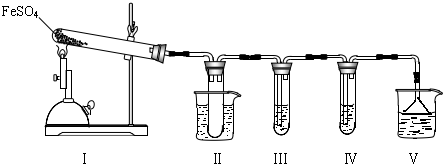
| 检验试剂 | 预期现象和结论 |
| 装置Ⅲ的试管中加入 | 产生大量白色沉淀,证明气体产物中含有SO3. |
| 装置Ⅳ的试管中加入 |
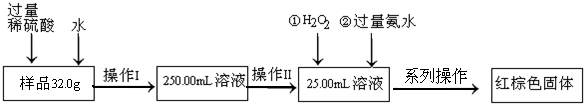
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、丝绸与棉布(采用灼烧闻其气味的方法) |
| B、Na2SO4与NH4Cl(采用加碱加热闻其气味的方法) |
| C、NaCl与KCl(采用灼烧时观察焰色的方法) |
| D、K2CO3与K2SO4(采用加BaCl2观察有无沉淀产生的方法) |
查看答案和解析>>
科目:高中化学 来源: 题型:
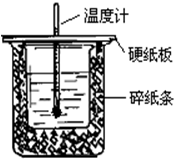 用50mL0.50mol/L盐酸与50mL0.55mol/LNaOH溶液在如图所示的装置中进行中和反应.通过测定反应过程中所放出的热量可计算中和热.回答下列问题:
用50mL0.50mol/L盐酸与50mL0.55mol/LNaOH溶液在如图所示的装置中进行中和反应.通过测定反应过程中所放出的热量可计算中和热.回答下列问题:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com