
����Ŀ��NaClO2��Ư��������Ư�۵�4��5���� NaClO2�㷺������ֽ��ҵ����ˮ�����ȡ���ҵ������NaClO2�Ĺ����������£�
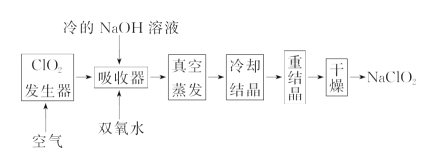
(1)ClO2���巢�����еķ�ӦΪ��2NaClO3��SO2��H2SO4===2ClO2��2NaHSO4��ʵ�ʹ�ҵ�����У�������ơ�Ũ�������ԭ���е�SO2����ԭ��Ϊ____________(�û�ѧ����ʽ��ʾ)��
(2)��Ӧ��������ClO2��������ͨ��һ����������Ŀ�ģ�________________________��
(3)������������NaClO2�����ӷ�Ӧ����ʽΪ________________________________��
(4)CO������(N2H4)�����ʼ�Ӧ�õ��о�����Դ������������������Ҫ���⡣
����CO��O2��KOH��Һ�����Ƴɼ���ȼ�ϵ�أ���õ�ط�Ӧ�����ӷ���ʽΪ_______________��
����CO��O2�������ʻ������Ƴ�����ͼ��ʾ��ȼ�ϵ�أ���缫d�ĵ缫��ӦʽΪ__________��
(5)���������������ڰ�����������ͨ��CuO��Һ�У��й����ʵ�ת����ͼ��ʾ��
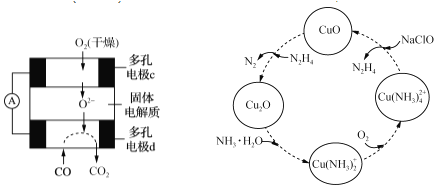
����ת��������ͨ������������Ӧ����Һ��pH��________(����������������С������������)��ת���е���1 mol N2H4���뷴Ӧʱ����Ҫ����O2�����ʵ���Ϊ________��
�ڼ���NaClOʱ�����ķ�ӦΪ��
Cu(NH3)42+��2ClO����2OH����Cu(OH)2����2N2H4����2Cl����2H2O
�÷�Ӧ����80�����Ͻ��У���Ŀ�ij��˼ӿ췴Ӧ�����⣬����_______________��
���𰸡�S��2H2SO4(Ũ)![]() 3SO2���� 2H2O���ϳ�ClO2��ȷ���䱻�������2ClO2��2OH����H2O2===2ClO2-��O2��2H2O2CO��O2��4OH��=== 2CO32����2H2OCO��O2����2e��===CO2����1mol������ͭ�ֽ⡢���������ܽ��ʹ�����Һ���ݳ�
3SO2���� 2H2O���ϳ�ClO2��ȷ���䱻�������2ClO2��2OH����H2O2===2ClO2-��O2��2H2O2CO��O2��4OH��=== 2CO32����2H2OCO��O2����2e��===CO2����1mol������ͭ�ֽ⡢���������ܽ��ʹ�����Һ���ݳ�
��������
(1)�������ȷ������еķ�ӦΪ�����������������Ũ���������·���������ԭ��Ӧ������ǡ�Ũ����Ҳ�������ɶ�������Ӧ�ķ���ʽΪ�� S��2H2SO4(Ũ)![]() 3SO2���� 2H2O��(2)��Ӧ���������������������������ȣ��ÿ������Խ����ų���ȷ���䱻������ա�(3)��������˫��ˮ����������ڼ��������·���������ԭ��Ӧ����NaClO2����Ӧ�����ӷ���ʽΪ��2ClO2��2OH����H2O2===2ClO2-��O2��2H2O��(4) �ٸ�ȼ�ϵ���и�����һ����̼ʧȥ���ӷ���������Ӧ���ɶ�����̼�������������õ��������ɻ�ԭ��Ӧ�������������ӣ�������̼�����������ӷ�Ӧ����̼������Ӻ�ˮ�����Ե�ط�ӦʽΪ��2CO��O2��4OH��= 2CO32����2H2O�� ��d�缫��һ����̼���ɶ�����̼����õ缫��ʧȥ���ӷ���������Ӧ���缫��ӦΪ CO��O2����2e��===CO2�� (5) ��Cu(NH3)42+��������Ӧ�����У�ͭԪ�ػ��ϼ���+1�۱�Ϊ+2�ۣ���Ԫ�ػ��ϼ۴�0�۱�Ϊ-2�ۣ������õ����Ӻ�ˮ��Ӧ�������������ӣ�������Һ��pH����ת���е���1molN2H4���뷴Ӧʱ��ת�Ƶ��ӵ����ʵ���Ϊ4mol������ת�Ƶ�����ȷ�������Ҫ�������������ʵ���Ϊ1mol���� �¶ȸ�ʱ������ͭ�ֽ⣬�������ܽ�����¶����߶����ͣ��Ӷ��ٽ���Ӧ������Ӧ������У��ʴ�Ϊ��������ͭ�ֽ⡢���������ܽ��ʹ�����Һ���ݳ���
3SO2���� 2H2O��(2)��Ӧ���������������������������ȣ��ÿ������Խ����ų���ȷ���䱻������ա�(3)��������˫��ˮ����������ڼ��������·���������ԭ��Ӧ����NaClO2����Ӧ�����ӷ���ʽΪ��2ClO2��2OH����H2O2===2ClO2-��O2��2H2O��(4) �ٸ�ȼ�ϵ���и�����һ����̼ʧȥ���ӷ���������Ӧ���ɶ�����̼�������������õ��������ɻ�ԭ��Ӧ�������������ӣ�������̼�����������ӷ�Ӧ����̼������Ӻ�ˮ�����Ե�ط�ӦʽΪ��2CO��O2��4OH��= 2CO32����2H2O�� ��d�缫��һ����̼���ɶ�����̼����õ缫��ʧȥ���ӷ���������Ӧ���缫��ӦΪ CO��O2����2e��===CO2�� (5) ��Cu(NH3)42+��������Ӧ�����У�ͭԪ�ػ��ϼ���+1�۱�Ϊ+2�ۣ���Ԫ�ػ��ϼ۴�0�۱�Ϊ-2�ۣ������õ����Ӻ�ˮ��Ӧ�������������ӣ�������Һ��pH����ת���е���1molN2H4���뷴Ӧʱ��ת�Ƶ��ӵ����ʵ���Ϊ4mol������ת�Ƶ�����ȷ�������Ҫ�������������ʵ���Ϊ1mol���� �¶ȸ�ʱ������ͭ�ֽ⣬�������ܽ�����¶����߶����ͣ��Ӷ��ٽ���Ӧ������Ӧ������У��ʴ�Ϊ��������ͭ�ֽ⡢���������ܽ��ʹ�����Һ���ݳ���


 �п������п��Ծ����ϵ�д�
�п������п��Ծ����ϵ�д� ��������״Ԫ��ϵ�д�
��������״Ԫ��ϵ�д� �ƸԿ�����ҵ��ϵ�д�
�ƸԿ�����ҵ��ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������й����ʷ���������ȷ��һ���ǣ�������
A. Ư���ǻ����� B. ˮ�����Ǵ�����
C. �����ǵ���� D. ������ڼ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������![]() ̼������Һ������Һ������Ũ�ȹ�ϵ������������ȷ����
̼������Һ������Һ������Ũ�ȹ�ϵ������������ȷ����![]() ����
����![]()
A. ![]()
![]()
B. ![]()
C. ![]()
![]()
D. ![]()
![]()
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������������ķ�����һ����ȵ���(����)
A. ������һ����̼��������ȣ��ܶȲ�ͬ
B. ������һ����̼������
C. ���¶���ͬ�������ȵ������������͵���
D. ��ѹǿ��ͬ�������ȵ������������͵���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����Ӧ![]() ��һ���ܱ������н��У����д�ʩ����ʹ��Ӧ����������ǣ� ��
��һ���ܱ������н��У����д�ʩ����ʹ��Ӧ����������ǣ� ��
����������![]() �������¶Ȣ�������䣬��ͨ��
�������¶Ȣ�������䣬��ͨ��![]() ����С�������ѹǿ��������䣬��ͨ��He��ѹǿ���䣬��ͨ��He
����С�������ѹǿ��������䣬��ͨ��He��ѹǿ���䣬��ͨ��He
A. ![]() B.
B. ![]() C.
C. ![]() D.
D. ![]()
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����л�ѧ���������ȷ���ǣ�
A. HCl �ĵ���ʽ��![]() B. F���ṹʾ��ͼ��
B. F���ṹʾ��ͼ�� ![]()
C. H2 ȼ�յ��Ȼ�ѧ����ʽ�� 2H2 (g) + O2 (g) = 2H2O (g) ��H = - 571.6 kJ��mol��1D. Cl2 ��ˮ��Ӧ�����ӷ���ʽ�� Cl2 + H2O = 2H+ +Cl�� + ClO-
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij��ȤС�����Ʊ���������֤��һϵ�����ʣ�ʵ��װ����ͼ��ʾ![]() ʡ�Լг�װ��
ʡ�Լг�װ��![]() ��֪�����������Na2S2O3��Һ�ڹ�ҵ�Ͽ���Ϊ���ȼ�
��֪�����������Na2S2O3��Һ�ڹ�ҵ�Ͽ���Ϊ���ȼ�

�ش��������⣺
��1������a��������______������ʢ��Ũ���ᣬ��ƿA��ʢ�еĹ����Լ���______![]() �ѧʽ
�ѧʽ![]() ��
��
��2��װ��B��ʢ�б���NaCl��Һ��װ��B��������______��
![]() ��ȥ
��ȥ![]() �е�����HCl
�����HCl![]() ����
���� ![]() �ṩ����ˮ����
�ṩ����ˮ���� ![]() �۲�װ���Ƿ����
�۲�װ���Ƿ����
��3��![]() ����ɫ������ɫ����d������ɫ����˵��______��
����ɫ������ɫ����d������ɫ����˵��______��
��4��ʵ�������e�Ļ�����ʹ���е���Һ���˵���ƿD�У�ҡ����ƿ�����ú�ɹ۲쵽______��
��5��װ��E�з�����Ӧ�����ӷ���ʽΪ______��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������ϲ��ؾ��п��������ס��������������������ã����Ľṹ��ʽ��ͼ��ʾ�������й������ϲ��ص�˵����ȷ����

A. �÷����к���1������̼ԭ��
B. 1mol�����ϲ���������2mol NaOH��Ӧ
C. 1mol �����ϲ���������2mol Br2��Ӧ
D. ����FeCl3��Һ������ɫ��Ӧ
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com