
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:2016-2017学年河北省高一上10月月考化学试卷(解析版) 题型:选择题
NA表示阿伏加德罗常数,下列说法正确的是
A.在常温常压下,11.2 LN2含有的分子数为0.5 NA
B.71gCl2所含原子数为NA
C.在常温常压下,1molNe含有的原子数为NA
D.在同温、同压下,相同体积的任何气体单质所含的原子数相同
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
| 反应时间 | CO2(mol) | H2(mol) | CH3OH(mol) | H2O(mol) | |
| 反应I 恒温恒容 | 0min | 2 | 6 | 0 | 0 |
| 10min | 4.5 | ||||
| 20min | 1 | ||||
| 30min | 1 | ||||
| 反应II 绝热恒容 | 0min | 0 | 0 | 2 | 2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 平衡常数减小 | B. | 物质A的转化率增加了 | ||
| C. | 平衡向逆反应方向移动了 | D. | a>b |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 22.9g/mol | B. | 26 | C. | 26 g/mol | D. | 29.3 g/mol |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 分子个数比为1:1 | B. | 原子个数比为5:4 | ||
| C. | 质量比为17:16 | D. | 氢原子个数比为4:3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
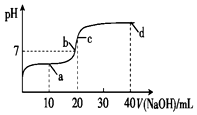 室温时,向20mL 0.1mol•L-1一元酸HA溶液中滴入0.1mol•L-1的NaOH溶液,溶液的pH变化曲线如图所示.下列说法正确的是( )
室温时,向20mL 0.1mol•L-1一元酸HA溶液中滴入0.1mol•L-1的NaOH溶液,溶液的pH变化曲线如图所示.下列说法正确的是( )| A. | a点:c(HA)>c(A-) | B. | b点:c(Na+)=c(A-)+c(HA) | ||
| C. | c点:c(H+)+c(HA)=c(OH-) | D. | d点:c(Na+)>c(A-)>c(OH-)>c(H+) |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
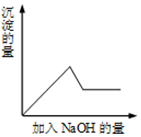 有一无色溶液,其中可能含有Fe3+、Cu2+、K+、Al3+、Mg2+、SO42-、Cl-等离子中的几种,为分析其成分,取此溶液分别进行了三个实验,其操作和有关现象如下:
有一无色溶液,其中可能含有Fe3+、Cu2+、K+、Al3+、Mg2+、SO42-、Cl-等离子中的几种,为分析其成分,取此溶液分别进行了三个实验,其操作和有关现象如下:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com