
【题目】已知:A为淡黄色固体,T、R为两种常见的用途很广的金属单质,D是具有磁性的黑色晶体,H是白色沉淀,且在潮湿空气中迅速变为灰绿色,最终变为红褐色固体。
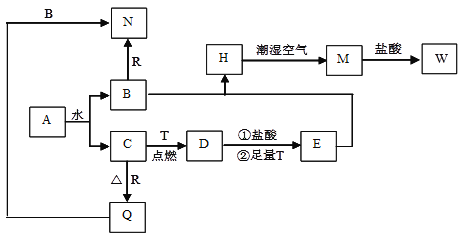
(1)写出下列物质的化学式A_______;D__________;N________。
(2)按要求写下列反应方程式:检验w中阳离子的离子方程式__________________________。
H在潮湿空气中变成M的化学方程式_________________________________。
D与盐酸反应的离子方程式_________________________________。
【答案】 Na2O2 Fe3O4 NaAlO2 Fe3++ 3OH- = Fe(OH)3↓或Fe3++ 3SCN- = Fe(SCN)3 4Fe(OH)2+O2+2H2O====4Fe(OH)3 Fe3O4+8H+====Fe2++2Fe3++ 4H2O
【解析】A为淡黄色固体,A为过氧化钠;D是具有磁性的黑色晶体,D为四氧化三铁;H是白色沉淀,且在潮湿空气中迅速变为灰绿色,最终变为红褐色固体,H为氢氧化亚铁;T、R为两种常见的用途很广的金属单质,可能为铁和铝,根据题意分析可知:T为铁,R为铝;过氧化钠与水反应生成氢氧化钠和氧气,氧气与铁反应生成四氧化三铁,四氧化三铁再与盐酸反应生成氯化亚铁、氯化铁和水,氯化铁溶液再与足量的铁反应生成氯化亚铁;过氧化钠与水反应生成氢氧化钠和金属铝反应生成偏铝酸钠和氢气;最后氯化亚铁溶液与氢氧化钠溶液反应生成氢氧化亚铁白色沉淀,在空气中氧化为氢氧化铁,最后和盐酸反应生成氯化铁溶液。
(1)根据以上分析可知:A为Na2O2、D为Fe3O4、N为NaAlO2;正确答案:Na2O2、Fe3O4、NaAlO2。
(2)w中阳离子为Fe3+,其检验方法为:滴加氢氧化钠溶液,生成红褐色沉淀,Fe3++ 3OH- = Fe(OH)3↓;或滴加硫氢化钾溶液,溶液变为血红色,Fe3++ 3SCN- = Fe(SCN)3;正确答案:Fe3++ 3OH- = Fe(OH)3↓或Fe3++ 3SCN- = Fe(SCN)3。氢氧化亚铁白色沉淀,在空气中氧化为氢氧化铁,化学方程式为4Fe(OH)2+O2+2H2O====4Fe(OH)3 ;正确答案:4Fe(OH)2+ O2+2H2O====4Fe(OH)3。四氧化三铁与盐酸反应生成氯化亚铁、氯化铁和水,反应的离子方程式:Fe3O4+8H+==Fe2++2Fe3++ 4H2O;正确答案:Fe3O4+8H+==Fe2++2Fe3++ 4H2O。


 状元及第系列答案
状元及第系列答案 同步奥数系列答案
同步奥数系列答案科目:高中化学 来源: 题型:
【题目】在探究新制饱和氯水成分的实验中,下列根据实验现象得出的结论不正确的是
A. 氯水的颜色呈浅黄绿色,说明氯水中含有Cl2
B. 向氯水中滴加硝酸酸化的AgNO3溶液,产生白色沉淀,说明氯水中含有Cl-
C. 向氯水中加入NaHCO3粉末,有气泡产生,说明氯水中含有H+
D. 向FeCl2溶液中滴加氯水,溶液颜色变成棕黄色,说明氯水中含有HCl
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某兴趣小组设计如图所示的装置进行原电池原理的探究。下列叙述错误的是
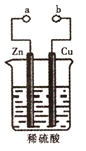
A. a和b不连接时,锌片上有气体生成,该装置不能形成原电池
B. a和b用导线连接时铜片为正极,发生的反应式为:2H++2e-=H2↑
C. a和b用导线连接时,电子由Zn经导线流向Cu,再经稀硫酸流回Zn
D. 无论a和b是否连接,稀硫酸均参与反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】三硫化磷(P4S3)是黄绿色针状晶体,易燃、有毒,分子结构之一如下图所示,已知其燃烧热ΔH=-3677 kJ/mol(P被氧化为P4O10),下列有关P4S3的说法不正确的是()

A. 分子中每个原子最外层均达到8电子稳定结构
B. P4S3中硫元素为-2价,磷元素为+3价
C. 一个P4S3分子中含有三个非极性共价键
D. 热化学方程式为:P4S3(s)+8O2(g)=P4O10(s)+3SO2(g) ΔH=-3677 kJ/mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】只能表示一个化学反应的离子方程式为
A. Ba2++SO42-=BaSO4↓ B. 2H++CO32-=H2O+CO2↑
C. Cl2+2Br-=2C1-+Br2 D. SO2+Br2+2H2O=4H++2Cl-+ SO42-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有关下列各装置图的叙述,不正确的是( )

A. 装置①可用于吸收实验中多余的Cl2
B. 装置②可用于收集H2、NH3、Cl2、HCl、NO等
C. 装置③中X为CCl4,可用于吸收氨气或氯化氢
D. 装置④可用于收集氨气,并吸收多余的氨气
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向x mL 2.0 mol·L-1的盐酸中投入a g镁铝合金,金属完全溶解,再加入y mL 1.0 mol·L-1的NaOH溶液沉淀达到最大值,且质量为(a+1.7) g,则下列说法不正确的是
A.x=2y
B.镁铝合金与盐酸反应时转移电子的数目为0.1NA
C.镁铝合金与盐酸反应产生H2的体积在常温常压下大于1.12 L
D.a的取值范围为0.9 g<a<1.2 g
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com