
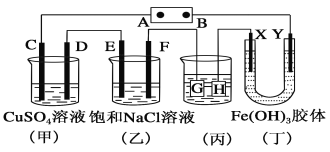
【题目】如图所示的装置,C、D、E、F、X、Y都是惰性电极。将电源接通后,向(乙)中滴入酚酞溶液,在F极附近显红色。则下列说法正确的是( )
A.电源B极是正极
B.(甲)(乙)装置的C、D、E、F电极均有单质生成,其物质的量之比为1∶2∶2∶1
C.欲用(丙)装置给铜镀银,H应该是Ag,电镀液是AgNO3溶液
D.装置(丁)中Y极附近红褐色变深,说明氢氧化铁胶粒带正电荷
【答案】D
【解析】
将直流电源接通后,F极附近呈红色,说明F极显碱性,是氢离子在该电极放电,所以F即是阴极,B是电源的负极,A是电源的正极,可得出D、F、H、Y均为阴极,C、E、G、X均为阳极。
A.根据上述分析可知B电极是电源的负极,A错误;
B.甲装置中,阳极C电极反应式为:4OH--4e-=O2↑+2H2O,阴极D电极反应式为:Cu2++2e-=Cu;乙装置是阳极E的电极反应为:2Cl--2e-=Cl2↑,阴极F电极的电极反应式为:2H++2e-=H2↑,当各电极转移电子均为1mol时,生成单质的量分别为:0.25mol、0.5mol、0.5mol、0.5mol,所以单质的物质的量之比为1:2:2:2,B错误;
C.电镀装置中,镀层金属必须作阳极,镀件作阴极,所以H应该是镀件,G是镀层金属,电解质溶液必须是含镀层金属离子的盐溶液,用(丙)装置给铜镀银,G应该是Ag,电镀液选用AgNO3溶液,C错误;
D.装置(丁)中Y极附近红褐色变深,证明氢氧化铁胶体微粒移向Y极,依据上述判断,X为阳极,Y为阴极,氢氧化铁胶体向Y电极移动,异性电荷相互吸引,所以氢氧化铁胶体粒子带正电荷,D正确;
故合理选项是D。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】关于该物质,下列说法正确的是()
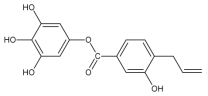
A.1mol该物质最多与8mol H2发生加成反应
B.1mol该物质最多与5mol Br2反应
C.1mol该物质最多与6mol NaOH发生反应
D.可以用酸性高锰酸钾溶液检验该物质中含有碳碳双键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在密闭容器中发生如下反应:aA(g)+bB(g)![]() cC(g)。其他条件不变时,改变某一条件对上述反应的影响,得到下列图像(图中p表示压强,T表示温度,n表示物质的量,α表示平衡转化率)。下列分析正确的是
cC(g)。其他条件不变时,改变某一条件对上述反应的影响,得到下列图像(图中p表示压强,T表示温度,n表示物质的量,α表示平衡转化率)。下列分析正确的是
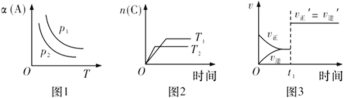
A.如图1反应:若p1>p2,则该反应只能在高温下自发进行
B.如图2反应:此反应的△H<0,且T1>T2
C.如图3反应:表示t1时刻可能是使用催化剂对反应速率的影响
D.如图3反应:表示t1时刻增大B的浓度对反应速率的影响
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】锌的化合物在工农业生产中有广泛的应用。请回答下列问题:
(1)基态锌原子中,核外电子占据的最高能级的符号是_________。锌的熔点比铝的熔点低,原因是______________。
(2)锌冶炼过程中会产生污染性气体二氧化硫,已知液态二氧化硫可以发生类似于水的自身电离2SO2(l)![]() SO2++
SO2++![]() ,S和O两种元素中电负性较强的是_______,与SO2+互为等电子体的单质分子为_______(填化学式),SO2+中的σ键和π键数目比为______________。
,S和O两种元素中电负性较强的是_______,与SO2+互为等电子体的单质分子为_______(填化学式),SO2+中的σ键和π键数目比为______________。
(3) [Zn(CN)4]2在水溶液中与HCHO发生如下反应:4HCHO+[Zn(CN)4]2+4H++4H2O![]() [Zn(H2O)4]2++4HOCH2CN,HOCH2CN分子中碳原子轨道的杂化类型是_________,HCHO的立体构型为_______________,[Zn(CN)4]2中Zn2+与CN中的C原子形成配位键,不考虑空间构型,[Zn(CN)4]2的结构可用示意图表示为__________________。
[Zn(H2O)4]2++4HOCH2CN,HOCH2CN分子中碳原子轨道的杂化类型是_________,HCHO的立体构型为_______________,[Zn(CN)4]2中Zn2+与CN中的C原子形成配位键,不考虑空间构型,[Zn(CN)4]2的结构可用示意图表示为__________________。
(4)硒化锌是一种重要的半导体材料,其晶胞结构如图所示,该晶胞中硒原子的配位数为_________。若该晶胞密度为ρ g·cm3,硒化锌的摩尔质量为M g/mol,NA代表阿伏加德罗常数,则晶胞参数a为__________cm。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一种形状像蝴蝶结的有机分子Bowtiediene,其形状和结构如图所示,下列有关该分子的说法中错误的是

A.1 mol 该物质彻底燃烧需要6 mol O2
B.三氯代物只有一种
C.该分子中所有碳原子在同一平面内
D.与其互为同分异构体,且官能团只含碳碳三键的链烃有两种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】盐卤中除含有Mg2+、Cl﹣外,还含有少量Na+、Fe2+、Fe3+、SO42﹣和CO(NH2)2等.从海水提取食盐和Br2后的盐卤中可以提取MgCl2、MgO、Mg(OH)2等物质,制备流程如图所示:

(1)从MgCl2溶液得到MgCl2.6H2O晶体的过程中所需的基本操作顺序依次为__________;
A 加热蒸馏 B 加热浓缩 C 冷却结晶 D 趁热过滤 E 过滤洗涤
(2)制取无水氯化镁必须在氯化氢存在的条件下进行,原因是___________(用适当的文字结合化学用语说明).
(3)用NaClO除去尿素CO(NH2)2时,生成物除盐外,都是能参与大气循环的物质,则该反应的化学方程式为___________;加入NaClO的另一个作用是___________.
(4)Mg(OH)2是制镁盐、耐火材料和阻燃剂的重要原料。
已知25℃时Ksp[Mg(OH)2]=5.6×10﹣12,且Mg(OH)2(s)═MgO(s)+H2O(s)△H=+81.5kJ/mol。
①下列叙述正确的是______
A.从盐卤或海水中获得Mg(OH)2,工业上选择NaOH作沉淀剂
B.Mg(OH)2能作阻燃剂的原因是它分解吸热且生成MgO覆盖可燃物
C.可加热Mg(OH)2得到MgO,再电解熔融的MgO制金属镁
②酸碱指示剂百里酚蓝变色的pH范围如下:
pH | <8.0 | 8.0~9.6 | >9.6 |
颜色 | 黄色 | 绿色 | 蓝色 |
25℃时,在Mg(OH)2的饱和溶液中滴加2滴百里酚蓝指示剂,溶液的颜色为___________.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】H2C2O4 是二元弱酸,常温下,Ka1(H2C2O4)=5.4×10-2,Ka2(H2C2O4)=5.4×10-4下列溶液的离子浓度关系式正确的是
A.pH=2的H2C2O4溶液中,c(H+)=c(HC2O4-)=10-2mol/L
B.pH=2的H2C2O4溶液与pH=12的NaOH溶液任意比例混合:c(Na+)+c(H+)=c(OH-)+c(HC2O4-)
C.将NaOH溶液滴加到H2C2O4溶液中至混合溶液呈中性:c(C2O42-)>c(HC2O4-)
D.NaHC2O4溶液中:c(Na+)>c(HC2O4-)>c(H2C2O4)>c(C2O42-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】药用有机化合物A(C8H8O2)为一种无色液体。从A出发可发生如图所示的一系列反应。则下列说法正确的是
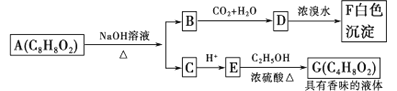
A.A的结构简式为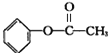
B.根据D和浓溴水反应生成白色沉淀可推知D为三溴苯酚
C.G的同分异构体中属于酯,且能发生银镜反应的只有一种
D.图中B→F与C→G发生反应的类型不相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】CPAE是蜂胶的主要活性成分,它可由咖啡酸合成,其合成过程如下。下列说法不正确的是

A. 咖啡酸的分子式为C9H8O4
B. 咖啡酸可发生加聚反应,并且所得聚合分子中含有3种官能团
C. 1 mol CPAE与足量的NaOH溶液反应,最多消耗3molNaOH
D. 1 mol CPAE与足量H2反应,最多消耗7 mol H2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com