
短周期元素E的氯化物ECln的熔点为-78℃,沸点为59℃;若0.2molECln与足量的AgNO3溶液完全反应后可以得到57.4g的AgCl沉淀。下列判断错误的是
A.E是一种非金属元素 B.在ECln中E与Cl之间形成共价键
C.E的一种常见氧化物为EO D.E位于元素周期表的ⅥA族
科目:高中化学 来源:2013-2014河南省洛阳市下学期期中考试高二化学试卷(解析版) 题型:选择题
可用于鉴别以下三种化合物的一组试剂是
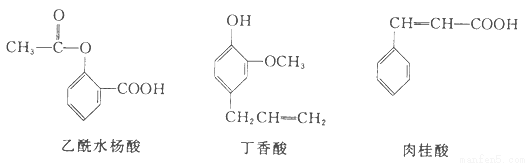
①银氨溶液②溴的四氯化碳溶液③氯化铁溶液④氢氧化钠溶液
A.①与② B.①与④ C.③与④ D.②与③
查看答案和解析>>
科目:高中化学 来源:2013-2014河南省安阳市高三毕业班第二次模拟理综化学试卷(解析版) 题型:简答题
碳、氮、氧、氟都是位于第二周期的重要的非金属元素。请回答下列问题:
(1)基态氟原子的核外电子排布式是______________ 。
(2)C、N、O、F四种元素第一电离能从大到小的顺序是_________________。
(3)碳和另外三种元素均可形成化合物。四氟化碳的空间构型为____________,CF4可以利用甲烷与Cl2和HF在一定条件下反应来制备,其反应方程式为___________;CO是__________分子(填“极性”或“非极性”),CO的常见等电子体为N2、CN-,已知CN-与N2结构相似,推算HCN分子中σ键与π键数目之比为___________;C3N4是一种新型材料,它的硬度比金刚石还高,可做切割工具,可推测出C3N4属于_________晶体。
(4)N4分子结构和白磷一样都是正四面体。又已知断裂1molN-N键吸收167kJ热量,生成1 molN≡N键放出942kJ热量,0.1 molN4转变为N2将放出____________热量:
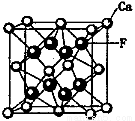
(5)CaF2和CaC2都属于离子晶体。CaF2晶体的密度为a g·cm-3,则晶胞(如图)的体积是_______________(只要求列出算式)。
(6)CaC2晶体的晶胞与氯化钠相似,但由于CaC2晶体中的C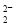 存在,使晶胞沿一个方向拉长,则CaC2晶体中1个C
存在,使晶胞沿一个方向拉长,则CaC2晶体中1个C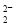 周围距离最近且相等的Ca2+数目为__________,C
周围距离最近且相等的Ca2+数目为__________,C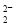 与O
与O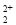 互为等电子体,O
互为等电子体,O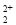 的电子式为____________。
的电子式为____________。
查看答案和解析>>
科目:高中化学 来源:2013-2014河南省商丘市高三第三次模拟考试理综化学试卷(解析版) 题型:选择题
下列说法正确的是
①NaHCO3溶液加水稀释,c(Na+)/ c(HCO3-)的比值保持增大
②浓度均为0.1 mol·L-1的Na2CO3、NaHCO3混合溶液:2c(Na+)=3[c(CO )+c(HCO
)+c(HCO )]
)]
③在0.1 mol·L-1氨水中滴加0.lmol·L-1盐酸,恰好完全中和时pH=a,则由水电离产生的
c(OH-)=l0-amol·L-1
④已知:Ksp(AgCl)=1.8xl0-10, Ksp(A92Cr2O4)=2.0×l0-12,则Ag2CrO4的溶解度小于AgCl
A.①④ B.②③ C.①③ D.②④
查看答案和解析>>
科目:高中化学 来源:2013-2014河南省周口市高一下学期期末考试化学试卷(解析版) 题型:实验题
实验室制备1,2-二溴乙烷的反应原理如下:
CH3CH2OH CH2=CH2+H2O
CH2=CH2+H2O
CH2=CH2+Br2→BrCH2CH2Br
可能存在的主要副反应有:乙醇在浓硫酸的存在下在140℃脱水生成乙醚;浓硫酸把乙醇氧化为CO2等。
用少量的溴和足量的乙醇制备1,2-二溴乙烷的装置如下图所示:
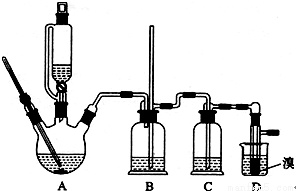
有关数据列表如下:
| 乙醇 | 1,2-二溴乙烷 | 乙醚 |
状态 | 无色液体 | 无色液体 | 无色液体 |
密度/g·cm3 | 0.79 | 2.2 | 0.71 |
沸点/oC | 78.5 | 132 | 34.6 |
熔点/oC | -130 | 9 | -116 |
回答下列问题:
(1)A装置上方使用滴液漏斗的优点是:_________________________;如果加热一段时间后发现忘记加瓷片,应该采取的正确操作是_____________________(填正确答案标号)。
A.立即补加 B.冷却后补加 C.不需补加 D.重新配料
(2)B装置的作用是_____________________________________。
(3)在装置C中应加入________(填正确选项前的字母),其目的是______________。
a.水 b.浓硫酸 c.氢氧化钠溶液 d.饱和碳酸氢钠溶液
(4)判断该制备反应已经结束的最简单方法是____________________________.
(5)D装置具支试管内若用溴水代替液溴(假定产物相同),分析其优点________________。
(6)反应过程中应用冷水冷却装置D,其主要目的是_____________;但又不能过度冷却(如用冰水),其原因是_________________________。
查看答案和解析>>
科目:高中化学 来源:2013-2014河南省周口市高一下学期期末考试化学试卷(解析版) 题型:选择题
设NA为阿伏加德罗常数,下列说法正确的是
A.若C2H6分子中含共价键数为7NA,则乙烷的体积为22.4L
B.58.5g氯化钠固体中含NaCl分子数为NA
C.78g液态苯分子中含碳碳双键数目为3NA
D.28gN2和6gH2在高温高压铁触媒催化作用下,生成的NH3分子数一定小于2NA
查看答案和解析>>
科目:高中化学 来源:2013-2014河南省周口市高一下学期期末考试化学试卷(解析版) 题型:选择题
下列反应既属于氧化还原反应,又是吸热反应的是
A.铝与稀盐酸的反应 B.甲烷在氧气中的燃烧反应
C.灼热的木炭与CO2反应 D.Ba(OH)2·8H2O晶体与NH4Cl晶体的反应
查看答案和解析>>
科目:高中化学 来源:2013-2014河南省周口市高二下学期6月联考化学试卷(解析版) 题型:选择题
某课外活动小组用如图所示装置进行实验(电解液足量)。

下列说法中错误的是
A.圈l中,若开始实验时开关K与a连接,则B极的电极反应式为
B.图l中,若开始实验时开关K与b连接,则一段时间后向电解液中通入适量HCl气体可恢复到电解前的浓
C.图2中,若开始实验时开关K与a连接,则电解液的溶质质量分数变小
D.图2中,若开始实验时开关K与b连接,则A极减少
的质量等于B极增加的质量
查看答案和解析>>
科目:高中化学 来源:2013-2014河南省周口市高一下学期5月联考化学试卷(解析版) 题型:选择题
下列物质中,在一定条件下能发生取代反应和加成反应,但不能使酸性高锰酸钾溶液褪色的是
A..苯 B.甲烷 C.乙烷 D.乙烯
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com