
 世纪百通期末金卷系列答案
世纪百通期末金卷系列答案科目:高中化学 来源: 题型:
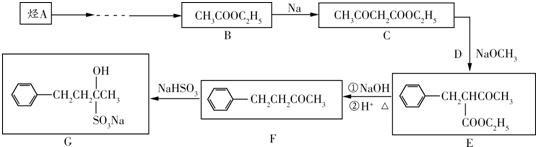
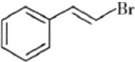 )具有强烈的类似素馨花青甜膏香,主要用于柏木,风信子,紫丁香,水仙,葵花香型皂用和洗衣粉香精中.以下是某课题组开发的从廉价、易得的化工原料出发制备E-β-溴代苏合香烯的合成路线:
)具有强烈的类似素馨花青甜膏香,主要用于柏木,风信子,紫丁香,水仙,葵花香型皂用和洗衣粉香精中.以下是某课题组开发的从廉价、易得的化工原料出发制备E-β-溴代苏合香烯的合成路线: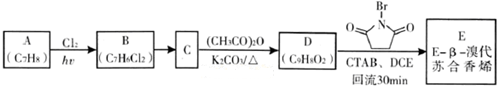
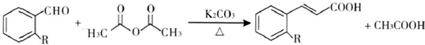
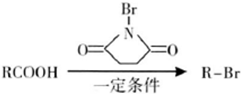
查看答案和解析>>
科目:高中化学 来源: 题型:
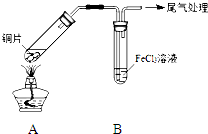 某校化学兴趣小组探究SO2与FeCl3溶液的反应,所用装置如图所示.
某校化学兴趣小组探究SO2与FeCl3溶液的反应,所用装置如图所示.| 步骤① | 配制1mol?L-1 FeCl3溶液(未用盐酸酸化),测其pH约为1,取少量装入试管B中,加热A. |
| 步骤② | 往5mL 1mol?L-1 FeCl3溶液中通入SO2气体,溶液立即变为红棕色.微热3min,溶液颜色变为浅绿色. |
| 步骤③ | 往5mL重新配制的1mol?L-1 FeCl3溶液(用浓盐酸酸化)中通入SO2气体,溶液立即变为红棕色.几分钟后,发现溶液颜色变成浅绿色. |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 酸或酶 |
| 酒化酶 |
| ①NaOH |
| ②H+△ |
查看答案和解析>>
科目:高中化学 来源: 题型:

| A、铜丝表面有气泡产生 |
| B、铁钉上发生的反应为:Fe-2e-=Fe2+ |
| C、一段时间后铁钉上出现红色物质 |
| D、如果把铜丝换成镁条,会加快铁钉的溶解 |
查看答案和解析>>
科目:高中化学 来源: 题型:
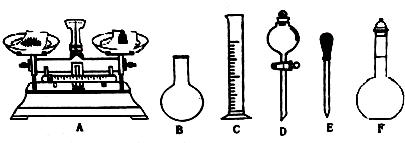
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、剩余40mL气体一定是O2 |
| B、剩余40mL气体是H2S或SO2 |
| C、混合气体中含H2S 40mL或80mL |
| D、剩余40mL气体是SO2和O2混合气体 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、二氧化硅晶体是一种无色透明的固体,常用作光导纤维的材料 |
| B、臭氧是一种有特殊臭味、氧化性极强的淡蓝色气体,可用作餐具的消毒剂 |
| C、铝及其合金是电气、工业、家庭广泛使用的材料,是因为铝比铁更耐酸、碱的腐蚀 |
| D、人造纤维可利用竹子、棉花、麻类的纤维材料制成,而合成纤维是利用自然界的非纤维材料(如石油、煤)通过化学合成方法得到 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Fe+4H++NO3-→Fe3++NO↑+2H2O |
| B、3Fe+8H++2 NO3-→3Fe2++2NO↑+4H2O |
| C、3Cu+8H++2 NO3-→3Cu2++2NO↑+4H2O |
| D、3Fe2++4H++NO3-→3Fe3++NO↑+2H2O |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com