
| ||
| 156×ng |
| 160 |
| ||
| m |
| 39n |
| 40m |
| 39n |
| 40m |


科目:高中化学 来源: 题型:
| A、Na++e--=Na |
| B、2H++4e-=2H2 |
| C、2Cl--2e-=Cl2 |
| D、4OH--4e-=2H2O+O2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、碳酸氢铵和足量的氢氧化钠溶液反应:NH4++OH-=NH3↑+H2O | ||||
| B、含等物质的量的硫酸氢钠与氢氧化钡两溶液混合:H++SO42-+Ba2++OH-=BaSO4↓+H2O | ||||
| C、用稀硝酸浸泡做过银镜反应的试管:3Ag+4H++NO3-=3Ag++NO↑+2H2O | ||||
D、用两个铜电极电解饱和食盐水:2Cl-+2H2O
|
查看答案和解析>>
科目:高中化学 来源: 题型:
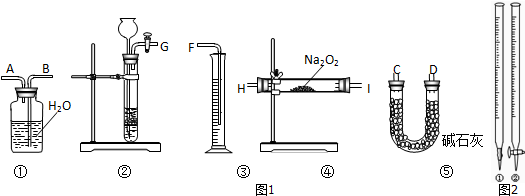
查看答案和解析>>
科目:高中化学 来源: 题型:


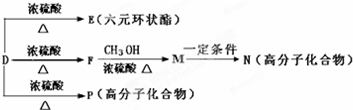
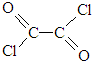 )与足量有机物D反应的化学方程式
)与足量有机物D反应的化学方程式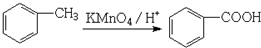

查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
 下面给出了四种烃A、B、C、D的相关信息:
下面给出了四种烃A、B、C、D的相关信息:查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
 如图是干冰的晶胞结构示意图.请完成下列问题:
如图是干冰的晶胞结构示意图.请完成下列问题:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com