
【题目】由CH3CH3→CH3CH2Cl→CH2 = CH2→CH3CH2OH的转化过程中,经过的反应是
A.取代→消去→加成 B.裂解→取代→消去
C.取代→加成→氧化 D.取代→消去→水解
科目:高中化学 来源: 题型:
【题目】常温下,某水溶液M中存在的离子有:Na+、A2-、HA-、H+、OH-,存在的分子有H2O、H2A。根据题意回答下列问题:
(1)写出酸H2A的电离方程式________________。
(2)若溶液M由10 mL 2 mol·L-1NaHA溶液与2 mol·L-1NaOH溶液等体积混合而成,则溶液M的pH________7(填“<”、“>”或“=”),溶液中离子浓度由大到小顺序为________________。已知常温下Ksp(BaA)=1.8×10-10,向该混合溶液中加入10 mL 1 mol·L-1BaCl2溶液,混合后溶液中的Ba2+浓度为__________ mol·L-1。
(3)若溶液M有下列三种情况:①0.01 mol·L-1的H2A溶液;②0.01 mol·L-1的NaHA溶液;③0.02 mol·L-1的HCl与0.04 mol·L-1的NaHA溶液等体积混合液,则三种情况的溶液中H2A分子浓度最大的为________;pH由大到小的顺序为_________________。
(4)若溶液M由pH=3的H2A溶液V1mL与pH=11的NaOH溶液V2mL混合反应而得,混合溶液c(H+)/c(OH-)=104,V1与V2的大小关系为_________(填“大于”“小于”“等于”或“均有可能”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铁元素及其化合物与人类的生产生活息息相关,试回答下列问题:
(1)电子工业常用30%的FeCl3溶液腐蚀敷在绝缘板上的铜箔,制造印刷电路板,该反应的离子方程式为_______________________。
(2)以H2、O2、熔融Na2CO3组成燃料电池,采用电解法制备Fe(OH)2,装置如图所示,其中P端通入CO2。
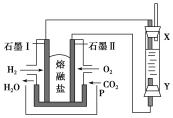
①石墨Ⅰ电极上的电极反应式为________________________________。
②通电一段时间后,右侧玻璃管中产生大量的白色沉淀,且较长时间不变色。则下列说法中正确的是________(填序号)。
A.X、Y两端都必须用铁作电极
B.可以用NaOH溶液作电解液
C.阴极发生的反应是2H2O+2e-===H2↑+2OH-
D.白色沉淀只能在阳极上产生
③若将所得Fe(OH)2沉淀暴露在空气中,其颜色变化为______________________________,该反应的化学方程式为________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】TiS2是镁电池的重要组成材料,其制备原理为Ti(SO4)2+8H2=TiS2+8H2O。下列说法正确的是
A. Ti(SO4)2失去电子B. H2被还原
C. H2是氧化剂D. Ti(SO4)2被还原
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各种描述中,正确的是 ( )
A.绿色食品是不含任何化学物质的食品
B.加碘食盐中所加的“碘”一般是碘化钾或碘单质
C.区别氯化铁溶液和氢氧化铁胶体可以用丁达尔效应
D.用干燥的有色布条可以检验氯化氢气体中是否混有氯气
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列表示物质或微粒的化学用语或模型正确的是
A. 中子数为8的碳原子: ![]() B. S2-的结构示意图:
B. S2-的结构示意图:
C. 二氧化碳电子式:![]() D. 氮气的结构式:N-N
D. 氮气的结构式:N-N
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列四种元素中,其单质氧化性最强的是( )。
A. 原子含有未成对电子最多的第2周期元素
B. 位于周期表第3周期ⅢA族的元素
C. 原子最外电子层排布式为2s22p6的元素
D. 原子最外电子层排布式为3s23p5的元素
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com