
| A、体积比为8:1 |
| B、分子个数之比为11:12 |
| C、物质的量之比为11:8 |
| D、原子个数之比为11:12 |
| m |
| M |
| m |
| M |


 巧学巧练系列答案
巧学巧练系列答案科目:高中化学 来源: 题型:
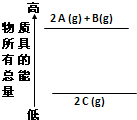
| A、2 A(g)+B(g)=2 C(g);△H<0 |
| B、2 A(g)+B(g)=2 C(g);△H>0 |
| C、2A+B=2 C;△H<0 |
| D、2C=2 A+B;△H<0 |
查看答案和解析>>
科目:高中化学 来源: 题型:
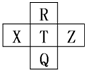 元素R、X、T、Z、Q在元素周期表中的相对位置如图所示,其中R单质在暗处与H2剧烈化合并发生爆炸.则下列判断正确的是( )
元素R、X、T、Z、Q在元素周期表中的相对位置如图所示,其中R单质在暗处与H2剧烈化合并发生爆炸.则下列判断正确的是( )| A、非金属性:T<X<R |
| B、气态氢化物稳定性:R<T<Q |
| C、R与Q的电子数相差16 |
| D、X与Q最高价氧化物的水化物的质子数相差18 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1,2,3-三甲基丁烷 |
| B、3-甲基-2-乙基丁烷 |
| C、2,3,3-三甲基-2-乙基己烷 |
| D、2,3,4-三甲基戊烷 |
查看答案和解析>>
科目:高中化学 来源: 题型:
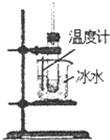 | 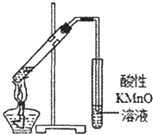 | 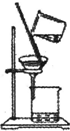 | 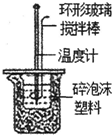 |
| A实验室制取少量的硝基苯 | B证明溴乙烷、NaOH、乙醇溶液共热生成乙烯 | C分离乙酸乙酯、碳酸钠和水的混合物 | D在实验室测定中和反应的反应热 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
 ,下列说法正确的是( )
,下列说法正确的是( )| A、R元素的原子序数为36 |
| B、R元素是第四周期元素 |
| C、R元素的最高正化合价为+8 |
| D、R元素的原子在反应中易失去电子 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、碳酸钙在水里的溶解度很小,所以碳酸钙是弱电解质 |
| B、NH3的水溶液导电,所以NH3是电解质 |
| C、强电解质在水溶液中的电离过程是不可逆的 |
| D、强电解质的水溶液导电能力一定比弱电解质的水溶液导电能力强 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1 mol FeI2与足量氯气反应时转移的电子数为2NA |
| B、2 L 0.5 mol?L-1硫酸钾溶液中阴离子所带电荷数为NA |
| C、1 mol Na2O2固体中含离子总数为4NA |
| D、丙烯和环丙烷组成的42 g混合气体中氢原子的个数为6NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1mol甲烷分子所含质子数、电子数均为10NA |
| B、1L0.1mol/L乙酸溶液中的H+离子数为0.1NA |
| C、24g镁原子最外层电子数为NA |
| D、标准状况下,22.4L乙醇的分子数等于NA |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com