
A、B、C、X均为中学常见的纯净物,它们之间有如下转化关系(副产物已略去)。
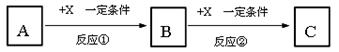
试回答:
(1)若X是强氧化性单质,则A不可能是________________。
a.S b.N2 c.Na d.Mg e.Al
(2)若X是金属单质,向C的水溶液中滴加AgNO3溶液,产生不溶于稀HNO3的白色沉淀,则B的化学式为________;以下选项中的试剂可以检验C溶液中金属阳离子的是__________(填字母编号)。
a.NaOH溶液 b.KSCN溶液 c.稀硫酸 d.新制氯水与KSCN溶液
C溶液在贮存时应加入少量金属单质X,理由是(用必要的文字和离子方程式表示
(3)若A、B、C为含有同种金属元素的无机化合物,X为强酸或强碱,A溶液与C溶液反应生成B。反应①的离子方程式可能为 或 。
科目:高中化学 来源: 题型:
将一支盛有a mL NO和b mL NO2气体的试管倒立于水槽中,然后通入a mL O2,问:
(1)若a=b,则充分反应后试管内气体体积为__________mL。
(2)若a<b,则充分反应后试管内气体体积为__________mL。
(3)若a>b,则充分反应后试管内气体体积为__________mL。
查看答案和解析>>
科目:高中化学 来源: 题型:
类推思维是化学解题中常用的一种思维方法,下列有关离子方程式的类推正确的是( )
|
| 已知 | 类推 |
| A | 将Fe加入CuSO4溶液中 Fe+Cu2+=Cu+Fe2+ | 将Na加入到CuSO4溶液中 2Na+Cu2+=Cu+2Na+ |
| B | 向稀硫酸加入NaOH溶液至中性 H++OH-=H2O | 向H2SO4溶液加入Ba(OH)2溶液至中性 H++OH-=H2O |
| C | 向氯化铝溶液中加入足量NaOH溶液 Al3+ + 4OH- = AlO2- + 2H2O | 向氯化铝溶液中加入足量氨水 Al3+ + 4NH3·H2O = AlO2- + 2H2O +4NH4+ |
| D | 向Ca(OH)2溶液中通入过量CO2 CO2 + OH- = HCO3- | 向Ca(OH)2溶液中通入过量SO2 SO2 + OH- = HSO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:
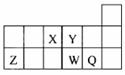
短周期元素X、Y、Z、W、Q在元素周期表中的相对位置如图所示。下列说法不正确的是( )
A.元素X与元素Z的最高正化合价之和的数值等于8
B.离子Y2-和Z 3+的核外电子数和电子层数均相同
C.元素W的最高价氧化物对应的水化物的酸性比Q的弱
D.元素X气态氢化物的稳定性大于元素Y的气态氢化物的稳定性
查看答案和解析>>
科目:高中化学 来源: 题型:
取少量MgO、Al2O3、SiO2、Fe2O3的混合粉末,加入过量盐酸,充分反应后过滤,得到固体X和滤液Y。下列叙述正确的是( )
A.上述四种氧化物中,至少有三种是碱性氧化物
B.将固体X加入氢氟酸中,X会溶解
C.滤液Y中的阳离子只有Mg2+、Al3+、Fe3+三种
D.滤液Y中加入过量氨水,所得沉淀为Fe(OH)3和Mg(OH)2
查看答案和解析>>
科目:高中化学 来源: 题型:
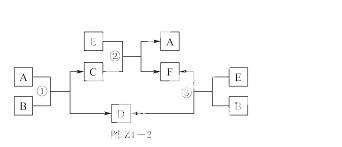
A、B、C、D、E、F六种物质在一定条件下有如图Z4-2所示的相互转化关系,所有反应物和生成物均已给出。
(1)若反应①、②、③均为溶液中的置换反应,A、D、E 为常见的金属单质,则 A 、D 、E 的还原性由强到弱的顺序为________________。
请写出满足以上要求的离子方程式:
反应①____________;反应②_____________。
(2)若反应①、②、③均为复分解反应。请写出满足要求的化学方程式:
反应①_ ____________________;
____________________;
反应②_____________________。
(3)若B是水,C是一种有磁性的化合物,E是一种无色、无味的有毒气体,则反应①的化学方程式是__________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
有一化合物X,可发生如下的转化关系(部分反应物、生成物省略)。其中B、D、E、F均为无色气体,W、K为常见的金属单质,C为难溶于水的红褐色固体。在混合液中加入BaCl2溶液可生成不溶于稀盐酸的白色沉淀,H和W反应可放出大量的热。
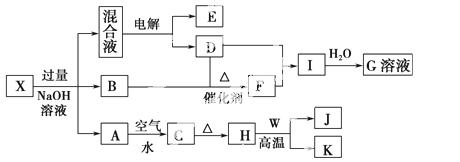
(1)X中滴入过量NaOH溶液的离子方程式为__________________________。
(2)I和水反应生成G的化学方程式为________________________________。
(3)I转化为G的反应中,当有2 mol G生成时,转移的电子数为_______________________________________________________________。
(4)引发H和W反应的操作是________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
用A+、B-、C2-、D、E、F、G和H分别表示含有18个电子的八种粒子(离子或分子),请回答:
(1)A元素是____、B元素是____、C元素是__(用元素符号表示)。
(2)D是由两种元素组成的双原子分子,其分子式是____。
(3)E是所有含18个电子的粒子中氧化能力最强的分子,其分子式是____。
(4)F是由两种元素组成的三原子分子,其分子式是____;电子式是____________。
(5)G分子中含有4个原子,其分子式是__________。
(6)H分子中含有8个原子,其分子式是______。
查看答案和解析>>
科目:高中化学 来源: 题型:
周期主族元素A、B、C、D、E、F的原子序数依次增大,它们的原
子核外电子层数之和为13。B的化合物种类繁多,数目庞大;C、D是空气中含量最多的两种元素,D、E两种元素的单质反应可以生成两种不同的离子化合物;F为同周期半径最小的元素。试回答以下问题:
(1)写出D与E以1∶1的原子个数比形成的化合物的电子式:________。F的原子结构示意图为:________。
(2)B、D形成的化合物BD2中存在的化学键为________键(填“离子”或“共价”,下同)。A、C、F三种元素形成的化合物CA4F为________化合物。
(3)化合物甲、乙由A、B、D、E中的三种或四种组成,且甲、乙的水溶液均呈碱性。则甲、乙反应的离子方程式为:____________________________________________。
(4)A、C、D、E的原子半径由大到小的顺序是________(用元素符号表示)。
(5)元素B和F的非金属性强弱,B的非金属性________于F(填“强”或“弱”),并用化学方程式证明上述结论___________________________________________________
________________________________________________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com