

 ,写出更改试剂(气体过量)后生成沉淀E所发生反应的离子方程式:AlO2-+CO2+2H2O=Al(OH)3↓+HCO3-.
,写出更改试剂(气体过量)后生成沉淀E所发生反应的离子方程式:AlO2-+CO2+2H2O=Al(OH)3↓+HCO3-.分析 合金中铝具有两性,能与氢氧化钠反应,故滤渣A是金属Fe和金属Cu,滤液中含有偏铝酸根离子,滤渣A中加入稀硫酸F溶解,Cu不溶解,故滤渣D使金属Cu,滤液C中含有亚铁离子,滤液B中加入适量HCl生成氢氧化铝沉淀,再加入适量盐酸变为氯化铝溶液;
(1)研磨成粉末可以增大反应物的接触面积,从化学反应速率方面考虑即可;
(2)铝、铁和铜三种金属中,只有金属铝能与氢氧化钠溶液反应,过滤后铁与稀硫酸反应生成硫酸亚铁和氢气,依据氧化还原反应原理书写方程式即可;
(3)氢氧化铝具有两性,即溶于强酸也溶于强碱,但是不溶于弱酸,据此解答即可;
(4)两种方法相比,二中生成二氧化硫污染环境,两个反应娿反应物与产物不同,则反应的热效应不同,以此来解答.
解答 解:(1)把合金研磨成合金粉,即把块状固体研磨成细小的颗粒,增大了反应物的接触面积,有利于反应进行,即加快了化学反应速率,
故答案为:增大反应物的接触面积,使反应速率加快;
(2)三种金属只有金属铝是两性金属,与氢氧化钠的溶液反应,反应生成氢气、偏铝酸钠,化学反应方程式为2Al+2NaOH+2H2O=2NaAlO2+3H2↑,过滤后铁与稀硫酸反应生成硫酸亚铁和氢气,反应方程式为Fe+H2SO4=FeSO4+H2↑,
故答案为:2Al+2NaOH+2H2O=2NaAlO2+3H2↑;Fe+H2SO4=FeSO4+H2↑;
(3)偏铝酸钠溶于过量的HCl会直接生成氯化铝而得不到氢氧化铝沉淀,氢氧化铝不溶于弱酸,故利用碳酸的弱酸性代替HCl,此气体为二氧化碳,电子式为: ,偏铝酸钠中通入过量的二氧化碳气体生成氢氧化铝沉淀和碳酸氢钠,离子反应方程式为:AlO2-+CO2+2H2O=Al(OH)3↓+HCO3-,
,偏铝酸钠中通入过量的二氧化碳气体生成氢氧化铝沉淀和碳酸氢钠,离子反应方程式为:AlO2-+CO2+2H2O=Al(OH)3↓+HCO3-,
故答案为: ;AlO2-+CO2+2H2O=Al(OH)3↓+HCO3-;
;AlO2-+CO2+2H2O=Al(OH)3↓+HCO3-;
(4)①两种方法相比可知,方法一,硫酸原料利用率高,对环境污染小,而方法二生成二氧化硫污染环境,则选择方法一,
故答案为:方法一,硫酸原料利用率高,对环境污染小;
②生成等量的硫酸铜两种方法消耗的能量不相同,则说法不正确,是因反应物与产物不完全相同,故反应的热效应不同,消耗的能量也不同,
故答案为:不正确;反应物与产物不完全相同,故反应的热效应不同,消耗的能量也不同.
点评 本题是对物质的分离和提纯知识点的考查,题目难度不是很大,掌握常见物质的制取方法以及氧化还原反应原理是解决本题的关键,注意整理.


科目:高中化学 来源: 题型:解答题
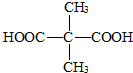 .
.
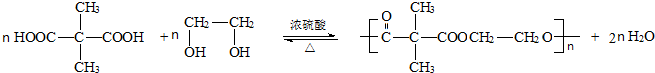 反应类型:缩聚反应.
反应类型:缩聚反应.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 硅太阳能电池工作时将光能转化为电能 | |
| B. | 物质之间发生化学反应时都会伴随着能量变化 | |
| C. | 催化剂虽然能降低反应的活化能,但不能改变反应的焓变 | |
| D. | 同温同压下,H2(g)+Cl2(g)═2HCl(g)在光照和点燃条件下的△H不同 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 不锈钢是利用牺牲阳极的阴极保护法来达到防止腐蚀的目的 | |
| B. | 明矾和漂白粉常用于自来水的净化和杀菌消毒,两者的作用原理相同 | |
| C. | 研究采煤、采油新技术,尽量提高产量以满足工业生产的快速发展 | |
| D. | “绿色化学”的核心是使原料可能全部转化为目标产物 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题

查看答案和解析>>
科目:高中化学 来源: 题型:填空题

查看答案和解析>>
科目:高中化学 来源: 题型:填空题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 利用电泳现象区别溶液和胶体 | |
| B. | 用滤纸过滤除去溶液中的胶体粒子 | |
| C. | 用渗析的方法除去胶体中的离子或分子,以净化胶体 | |
| D. | 向Fe(OH)3胶体中加入足量AgNO3溶液,以除去胶体中的CI- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | H2SO4=H22++SO42- | B. | NaHCO3=Na++H++CO32- | ||
| C. | NaOH=Na++O2-+H+ | D. | Na3PO4=3Na++PO43- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com