
| A. | 常温常压下6.0g乙酸所含σ键数目为0.8NA | |
| B. | 2.0gH218O与D2O的混合物中所含中子数为NA | |
| C. | 标准状况下,5.6LCO2与足量Na2O2反应转移的电子数为0.5NA | |
| D. | 50mLl2mol/L盐酸与足量MnO2共热,转移的电子数为0.3NA |
分析 A、求出乙酸的物质的量,然后根据乙酸中含7条σ键来分析;
B、H218O与D2O的摩尔质量均为20g/mol,且均含10个中子;
C、求出二氧化碳的物质的量,然后根据过氧化钠和二氧化碳反应时,1mol二氧化碳参与反应,反应转移1mol电子;
D、二氧化锰只能与浓盐酸反应,和稀盐酸不反应.
解答 解:A、6.0g乙酸的物质的量为0.1mol,而乙酸中含7条σ键,故0.1mol乙酸中含0.7NA条σ键,故A错误;
B、H218O与D2O的摩尔质量均为20g/mol,故2.0g混合物的物质的量为0.1mol,且两者均含10个中子,故0.1mol混合物中含NA个中子,故B正确;
C、标况下5.6L二氧化碳的物质的量为0.25mol,而过氧化钠和二氧化碳反应时,1mol二氧化碳参与反应,反应转移1mol电子,故当0.25mol二氧化碳反应时,反应转移0.25NA个电子,故C错误;
D、二氧化锰只能与浓盐酸反应,和稀盐酸不反应,故盐酸不能反应完全,则转移的电子数小于0.3NA个,故D错误.
故选B.
点评 本题考查了阿伏伽德罗常数的有关计算,难度不大,应注意掌握公式的运用和物质的结构.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 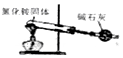 实验室用如图装置来制取NH3 | B. | 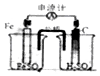 实验如图碳棒上有无色气泡产生 | ||
| C. | 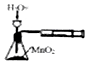 实验如图定量测定H2O2的分解速率 | D. |  实验如图检验钾元素 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 光导纤维的主要成分是SiO2,太阳能电池的主要成分是单质硅 | |
| B. | 墨水是一种胶体,不同墨水混用时可能使铭笔流水不畅或者堵塞 | |
| C. | 食品包装袋内常用硅胶、生石灰和还原铁粉,其作用相同 | |
| D. | 用铝制容器盛装浓硫酸的原因是其表面发生钝化反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | M、Q、R 三种元素组成的物质中只含共价键 | |
| B. | 碳元素与 R 元素形成的原子个数比为 1:1 的化合物只有 1 种 | |
| C. | X 单质常温下与 M 单质反应,生成 X2M2 | |
| D. | QMX 是形成酸雨和雾霾的原因之一 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ③⑥⑦ | B. | ①③⑤ | C. | ①②④ | D. | ④⑤⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 自来水厂用明矾净水,用Fe2(SO4)3或ClO2均能代替明矾净水 | |
| B. | 青篙素在超临界CO2中有很强的溶解性,萃取青蒿素可用超临界CO2作萃取剂 | |
| C. | 用石灰水或MgSO4溶液喷涂在树干上均可消灭树皮上的过冬虫卵 | |
| D. | 新型材料聚碳酸酯纤维、石墨烯纤维都属于有机高分子 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 热稳定性:HF、NH3、SiH4依次增大 | |
| B. | 原子半径:C、Al、K依次增大 | |
| C. | 酸碱性:NaOH、Al(OH)3、Mg(OH)2碱性减弱 | |
| D. | 非金属性:Cl、S、P依次增强 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题

| 实验步骤 | 实验操作 | 现象 | 实验结论 |
| 1 | ① | ② | NaNO2具有氧化性 |
| 2 | ③ | ④ | NaNO2具有还原性 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com