
| �¶�/�� | 0 | 20 | 80 | 100 |
| �ܽ�ȣ�g/100g H2O�� | 74.4 | 91.8 | 525.8 | 535.7 |
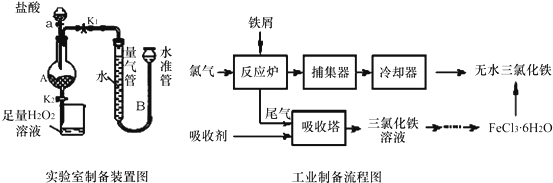
���� ��1������ʵ��װ�úͲ��������֪���ձ���������H2O2��Һ����������������������ȫ�����������������ӣ�
��2��Ϊ�˲ⶨ����м�������������������������������ȫ��Ӧ�����ٲ������������жϣ�
��3����FeCl3��Һ�Ƶ�FeCl3•6H2O����IJ��������ǣ�����Ũ������ȴ�ᾧ�����ˡ�ϴ�ӡ����
��4���������������������ռ����գ���Ӧ������2FeCl3��Һ���ݴ���д���ӷ���ʽ��
��5��������Է�������Ϊ325��FeCl3����Է���������162.5�ƶϸ����ʵķ���ʽ��
��6���ٸ����� Na2S2O3��Һ�ζ�����Һ�ж���ƿ�ڵ���Һ����ɫ��Ϊ��ɫ���Ұ�����ڲ���ɫ�ж��յ㣻
�ڸ��ݻ�ѧ����ʽ����Ʒ���Ȼ���������������
��� �⣺��1������ʵ��װ�úͲ��������֪��ʵ�����Ʊ���ˮFeCl3���������������ᷴӦ����FeCl2��Ȼ���FeCl2������FeCl3�����Ƶ�FeCl3•6H2O���壬���ѽᾧˮ�Ƶ���ˮFeCl3���ձ���������H2O2��Һ����������������������ȫ�����������������ӣ�
�ʴ�Ϊ������������ȫ�����������������ӣ�
��2���������ᷴӦ��ȫʱ�����ٲ�������������װ��A�в��������ݻ������ܺ�ˮ�ܵ�Һ�治�ٱ仯����ʱ���ɽ�A��FeCl2��Һ�����ձ��н���������
�ʴ�Ϊ��װ��A�в��������ݻ������ܺ�ˮ��Һ�治�䣻
��3����FeCl3��Һ�Ƶ�FeCl3•6H2O���壬Ϊ�˷�ֹFeCl3��Һ����ˮ�⣬���ȼ������ᣬ��������Ũ������ȴ�ᾧ�����ˡ�ϴ�ӡ�����ʴ�Ϊ���������Ũ������ȴ�ᾧ��
��4���ӹ�ҵ�Ʊ�����ͼ������֪����Ӧ¯�н��еķ�Ӧ�� 2Fe+3Cl2=2FeCl3����ˣ������������е�β����û�вμӷ�Ӧ���������������������������ռ����գ���Ӧ������2FeCl3��Һ���������ռ�Ӧ��2FeCl2��Һ����Ӧ�����ӷ���ʽΪ��2Fe2++Cl2=2Fe3++2Cl-��
�ʴ�Ϊ��2Fe2++Cl2=2Fe3++2Cl-��
��5���������ռ�������̬FeCl3��FeCl3����Է���������162.5������Է�������Ϊ325�������Ȼ�������Ƴ������¶ȳ���673Kʱ����������̬FeCl3���Ծۺ�����˫����Fe2Cl6��
�ʴ�Ϊ��Fe2Cl6��
��6���ٳ�ȡm g��ˮ�Ȼ�����Ʒ������ϡ���ᣬ���Ƴ�100mL��Һ��ȡ��10.00mL�������Թ�����KI��Һ����ַ�Ӧ���뼸�ε�����Һ����ʱ��Һ����ɫ���� Na2S2O3��Һ�ζ����������һ��Na2S2O3��Һ����ƿ�ڵ���Һ����ɫ��Ϊ��ɫ���Ұ�����ڲ���ɫ�����Եζ��յ�������ǣ���Һ����ɫ��Ϊ��ɫ���Ұ�����ڲ���ɫ����
�ʴ�Ϊ����Һ����ɫ����ɫ���Ұ�����ڲ���ɫ��
������Ʒ���Ȼ�������������
�ɷ�Ӧ��2Fe3++2I -=2Fe2++I2�� I2+2S2O32-�T2I-+S4O62-���ɵù�ϵʽ��
2Fe3+-I2-2S2O32-
1 1
n cV��10-3
���n��Fe3+��=cV��10-3mol������Ʒ���Ȼ�������������Ϊ��
�أ�Fe3+��=cV��10-3mol��10��162.5g/mol��100%=$\frac{162.5cV}{m}$%��
�ʴ�Ϊ��$\frac{162.5cV}{m}$%��
���� ���⿼��ѧ���Թ������̵����⡢���ʵķ����ᴿ�Ȼ���������������ԭ��Ӧ�ζ�Ӧ�á��ܶȻ��йؼ���ȣ��Ѷ��еȣ���Ҫѧ��������ʵ�Ļ���֪ʶ���������֪ʶ��������������


 ѧ�����νӽ̲��Ͼ���ѧ������ϵ�д�
ѧ�����νӽ̲��Ͼ���ѧ������ϵ�д� Сѧ������ҵϵ�д�
Сѧ������ҵϵ�д� ��ʿһ��ȫͨϵ�д�
��ʿһ��ȫͨϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
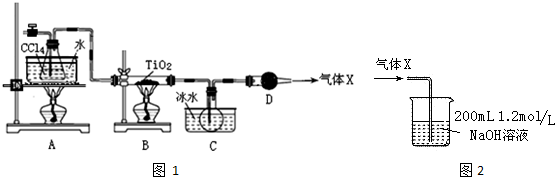
| ���� | �۵�/�� | �е�/�� | ���� |
| CCl4 | -23 | 76.8 | ��TiCl4���� |
| TiCl4 | -25 | 136 | ����ʪ������������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
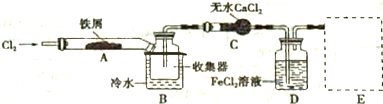

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | CxHy��l��+��x+$\frac{y}{4}$��O2��g��=xCO2��g��+$\frac{y}{2}$H2O��l����H=��$\frac{10Q}{9}$-1366.8��kJ•mol-1 | |
| B�� | CxHy��l��+��x+$\frac{y}{4}$��O2��g��=xCO2��g��+$\frac{y}{2}$H2O��l����H=��-$\frac{10Q}{9}$+1366.8��kJ•mol-1 | |
| C�� | CxHy��l��+��x+$\frac{y}{4}$��O2��g��=xCO2��g��+$\frac{y}{2}$H2O��l����H=��$\frac{10Q}{9}$-151.9��kJ•mol-1 | |
| D�� | CxHy��l��+��x+$\frac{y}{4}$��O2��g��=xCO2��g��+$\frac{y}{2}$H2O��l����H=��-$\frac{10Q}{9}$+151.9��kJ•mol-1 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��a+b��c+d������ѹǿ����ƽ�������ƶ� | |
| B�� | ��������Ӧ��ʼ����ʼʱA��B�����ʵ���֮��Ϊa��b����ƽ��ʱA��B��ת����֮��Ϊa��b | |
| C�� | ��a+b=c+d����ƽ����ϵ�й�������m mol���������г���n mol B����ﵽƽ��ʱ���������ʵ���С�ڣ�m+n��mol | |
| D�� | ��a+b=c+d��������������������������¶ȣ�ƽ�������ƶ�������������ѹǿ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
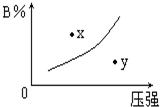 ��ӦmA��s��+nB��g��?pC��g����H=-QkJ/mol��һ���¶���B�����������B%����ѹǿ�仯�Ĺ�ϵ��ͼ��ʾ��������������ȷ���ǣ�������
��ӦmA��s��+nB��g��?pC��g����H=-QkJ/mol��һ���¶���B�����������B%����ѹǿ�仯�Ĺ�ϵ��ͼ��ʾ��������������ȷ���ǣ�������| A�� | ֻ�Т� | B�� | ֻ�Тڢ� | C�� | ֻ�Т٢ڢ� | D�� | ֻ�Тٺ͢� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com